Bài 5 trang 139 SGK Hoá 11 Cánh diều: Chuẩn Độ Axit Acetic Trong Giấm
11:01:57Cập nhật: 27/08/2025
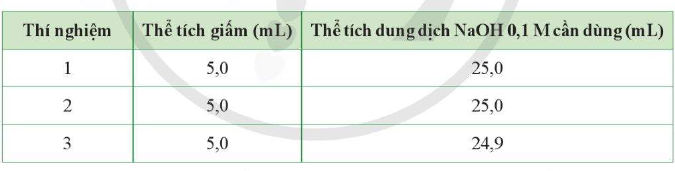
Bài 5 trang 139 Hóa 11 là một bài toán thực tế thuộc chủ đề 6 "Carboxylic acid" sách Cánh diều. Bài tập này giúp các em củng cố kiến thức về phương pháp chuẩn độ và cách tính nồng độ của một dung dịch.
Bài toán này giúp các em làm quen với phương pháp chuẩn độ trong hóa học phân tích. Nắm vững công thức tính nồng độ và cách xác định thể tích trung bình từ các thí nghiệm thực tế là chìa khóa để giải quyết các bài toán tương tự. Chúc các em học tốt!
• Xem hướng dẫn giải Hoá 11 SGK Cánh diều cùng chuyên mục
> Bài 2 trang 139 Hoá 11 Cánh diều: Chất nào sau đây có nhiệt độ sôi cao nhất? A. Propan – 1 – ol...
Đánh giá & nhận xét
Tin liên quan
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo Bài 5 trang 91 SGK Hoá 11 Cánh diều
Bài 5 trang 91 SGK Hoá 11 Cánh diều Bài 4 trang 91 SGK Hoá 11 Cánh diều
Bài 4 trang 91 SGK Hoá 11 Cánh diều Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene Bài 2 trang 91 SGK Hoá 11 Cánh diều
Bài 2 trang 91 SGK Hoá 11 Cánh diều Bài 1 trang 91 SGK Hoá 11 Cánh diều
Bài 1 trang 91 SGK Hoá 11 Cánh diều Bài 6 trang 99 SGK Hoá 11 Cánh diều
Bài 6 trang 99 SGK Hoá 11 Cánh diều Bài 5 trang 99 SGK Hoá 11 Cánh diều
Bài 5 trang 99 SGK Hoá 11 Cánh diều Bài 4 trang 99 SGK Hoá 11 Cánh diều
Bài 4 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 99 SGK Hoá 11 Cánh diều
Bài 3 trang 99 SGK Hoá 11 Cánh diều Bài 2 trang 99 SGK Hoá 11 Cánh diều
Bài 2 trang 99 SGK Hoá 11 Cánh diều Bài 1 trang 99 SGK Hoá 11 Cánh diều
Bài 1 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học Bài 2 trang 106 SGK Hoá 11 Cánh diều
Bài 2 trang 106 SGK Hoá 11 Cánh diều Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen Bài 5 trang 71 SGK Hoá 11 Cánh diều
Bài 5 trang 71 SGK Hoá 11 Cánh diều Bài 4 trang 71 SGK Hoá 11 Cánh diều
Bài 4 trang 71 SGK Hoá 11 Cánh diều Bài 3 trang 71 SGK Hoá 11 Cánh diều
Bài 3 trang 71 SGK Hoá 11 Cánh diều Bài 2 trang 71 SGK Hoá 11 Cánh diều
Bài 2 trang 71 SGK Hoá 11 Cánh diều Bài 1 trang 71 SGK Hoá 11 Cánh diều
Bài 1 trang 71 SGK Hoá 11 Cánh diều Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Tin mới
Tin cùng chuyên mục
Tin xem nhiều nhất