Bài 2 trang 106 SGK Hoá 11 Cánh diều
Bài tập số 2, trang 106 SGK Hóa học 11 (Cánh Diều), là bài toán quan trọng về tổng hợp polymer trong công nghiệp, cụ thể là PVC (Polyvinyl chloride). PVC là một trong những loại nhựa được ứng dụng rộng rãi nhất. Sơ đồ phản ứng tổng hợp PVC bao gồm chuỗi các phản ứng chuyển hóa từ methane (CH4) thành monomer vinyl chloride (CH2=CHCl).
Bài 2 trang 106 Hoá 11 Cánh diều:
PVC là một trong những polymer được ứng dụng nhiều trong đời sống và sản xuất. Hoàn thành sơ đồ phản ứng tổng hợp PVC dưới đây:
Phân Tích Hướng Dẫn Giải:
Để tổng hợp $\text{PVC}$, ta cần đi qua 3 bước chính:
-
Phản ứng (1): Chuyển hóa $\text{CH}_4$ thành acetylene ($\text{C}_2\text{H}_2$ / $\text{CH}\equiv\text{CH}$) bằng phương pháp nhiệt phân.
-
Phản ứng (2): Chuyển hóa $\text{C}_2\text{H}_2$ thành vinyl chloride ($\text{CH}_2=\text{CHCl}$) bằng phản ứng cộng $\text{HCl}$.
-
Phản ứng (3): Trùng hợp monomer $\text{CH}_2=\text{CHCl}$ để tạo thành polymer $\text{PVC}$.
Giải bài 2 trang 106 Hoá 11 Cánh diều:
Hoàn thành sơ đồ phản ứng tổng hợp PVC
2CH4 CH ≡ CH + 3H2
CH ≡ CH + HCl CH2 = CHCl
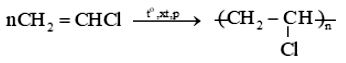
Hay có thể viết:
$CH_4$ $CH\equiv CH$
$CH_2=CHCl$
$PVC$
Sơ đồ tổng hợp $\text{PVC}$ trong công nghiệp được hoàn thành qua ba giai đoạn chính: (1) Nhiệt phân $\text{CH}_4$ tạo $\text{C}_2\text{H}_2$; (2) Cộng $\text{HCl}$ vào $\text{C}_2\text{H}_2$ tạo ra monomer vinyl chloride ($\text{CH}_2=\text{CHCl}$); (3) Trùng hợp monomer để tạo thành polymer $\text{PVC}$.
• Xem thêm:
Đánh giá & nhận xét
-
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Bài 5 trang 91 SGK Hoá 11 Cánh diều
Bài 5 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 91 SGK Hoá 11 Cánh diều
Bài 4 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
-
 Bài 2 trang 91 SGK Hoá 11 Cánh diều
Bài 2 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 91 SGK Hoá 11 Cánh diều
Bài 1 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 6 trang 99 SGK Hoá 11 Cánh diều
Bài 6 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 5 trang 99 SGK Hoá 11 Cánh diều
Bài 5 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 99 SGK Hoá 11 Cánh diều
Bài 4 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 99 SGK Hoá 11 Cánh diều
Bài 3 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 2 trang 99 SGK Hoá 11 Cánh diều
Bài 2 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 99 SGK Hoá 11 Cánh diều
Bài 1 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
-
 Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
-
 Bài 5 trang 71 SGK Hoá 11 Cánh diều
Bài 5 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 71 SGK Hoá 11 Cánh diều
Bài 4 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 71 SGK Hoá 11 Cánh diều
Bài 3 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 2 trang 71 SGK Hoá 11 Cánh diều
Bài 2 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 71 SGK Hoá 11 Cánh diều
Bài 1 trang 71 SGK Hoá 11 Cánh diều
-
 Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 2 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 2 trang 71 Hóa 11 Cánh Diều SGK


















































