Bài 6 trang 99 SGK Hoá 11 Cánh diều
Bài tập số 6, trang 99 SGK Hóa học 11 (Cánh Diều), là bài toán quan trọng về phản ứng nitro hóa toluene để điều chế 2,4,6-trinitrotoluene ($\text{TNT}$), một loại thuốc nổ mạnh. Bài toán bao gồm cả việc viết phương trình hóa học và tính toán khối lượng sản phẩm theo hiệu suất.
Bài 6 trang 99 Hoá 11 Cánh diều:
2,4,6-trinitrotoluene dùng để sản xuất thuốc nổ TNT.
a) Viết phương trình hoá học của phản ứng điều chế 2,4,6-trinitrotoluene từ toluene và nitric acid (xúc tác sulfuric acid).
b) Từ 1 tấn toluene điều chế được bao nhiêu kg 2,4,6-trinitrotoluene, biết hiệu suất của phản ứng là 62%.
Phân Tích Hướng Dẫn Giải:
-
Phản ứng (a): Phản ứng nitro hóa toluene. Nhóm $\text{-CH}_3$ định hướng thế vào các vị trí ortho và para. Để thế cả ba nhóm nitro ($\text{-NO}_2$), cần hỗn hợp acid mạnh ($\text{H}_2\text{SO}_4$ đặc và $\text{HNO}_3$ đặc) và nhiệt độ cao.
-
Tính khối lượng (b):
-
Thiết lập tỉ lệ khối lượng theo phương trình hóa học.
-
Tính khối lượng sản phẩm theo lí thuyết ($\text{m}_{\text{LT}}$).
-
Áp dụng công thức hiệu suất: $\text{m}_{\text{TT}} = \text{m}_{\text{LT}} \cdot H\%$.
-
Giải bài 6 trang 99 Hoá 11 Cánh diều:
a) Phương trình hoá học điều chế 2,4,6-trinitrotoluene từ toluene và nitric acid
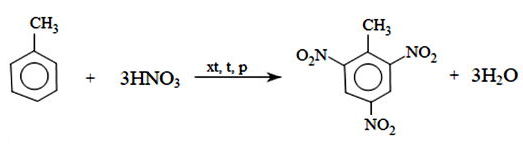
b) Ta có sơ đồ:
C6H5 – CH3 → C6H2(NO2)3CH3
92 227 (gam)
1 tấn m (tấn)
Suy ra:
$m=\frac{1.227}{92}.62%$ $=\frac{227}{92}.\frac{62}{100}$ $=1,53(tấn) = 1530 (kg)$
-
Phương trình Phản ứng: Phản ứng nitro hóa toluene là $\mathbf{\text{C}_6\text{H}_5\text{CH}_3 + 3\text{HNO}_3 \xrightarrow{\text{H}_2\text{SO}_4 \text{ đặc}, t^\circ} \text{C}_6\text{H}_2(\text{NO}_2)_3\text{CH}_3 + 3\text{H}_2\text{O}}$.
-
Khối lượng TNT: Áp dụng hiệu suất $62\%$, khối lượng $\text{TNT}$ thực tế thu được từ 1 tấn toluene là $\mathbf{1530 \text{ kg}}$
• Xem thêm:
Đánh giá & nhận xét
-
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
-
 Bài 5 trang 91 SGK Hoá 11 Cánh diều
Bài 5 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 91 SGK Hoá 11 Cánh diều
Bài 4 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
-
 Bài 2 trang 91 SGK Hoá 11 Cánh diều
Bài 2 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 91 SGK Hoá 11 Cánh diều
Bài 1 trang 91 SGK Hoá 11 Cánh diều
-
 Bài 5 trang 99 SGK Hoá 11 Cánh diều
Bài 5 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 99 SGK Hoá 11 Cánh diều
Bài 4 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 99 SGK Hoá 11 Cánh diều
Bài 3 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 2 trang 99 SGK Hoá 11 Cánh diều
Bài 2 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 99 SGK Hoá 11 Cánh diều
Bài 1 trang 99 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
-
 Bài 2 trang 106 SGK Hoá 11 Cánh diều
Bài 2 trang 106 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
-
 Bài 5 trang 71 SGK Hoá 11 Cánh diều
Bài 5 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 4 trang 71 SGK Hoá 11 Cánh diều
Bài 4 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 3 trang 71 SGK Hoá 11 Cánh diều
Bài 3 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 2 trang 71 SGK Hoá 11 Cánh diều
Bài 2 trang 71 SGK Hoá 11 Cánh diều
-
 Bài 1 trang 71 SGK Hoá 11 Cánh diều
Bài 1 trang 71 SGK Hoá 11 Cánh diều
-
 Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
-
 Giải bài 2 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 2 trang 71 Hóa 11 Cánh Diều SGK


















































