Vậy dẫn xuất halogen của hiđrocacbon là gì? có tính chất hóa học và tính chất vật lý ra sao? được ứng dụng vào những lĩnh vực nào trong đời sống? chúng ta cùng tìm hiểu qua bài viết dưới đây.
I. Khái niệm, phân loại
1. Khái niệm dẫn xuất halogen
• Khi thay thế nguyên tử hiđro của phân tử hiđrocacbon bằng nguyên tử halogen ta được dẫn xuất halogen của hiđrocacbon.
| Hiđrocacbon | CH4 | CH2=CH2 | C6H6 |
| Dẫn xuất halogen | CH3Cl, CH3Br, CH2Cl2, CH2ClF | CH2=CH-Cl | C6H5Cl |
- Thay thế' nhóm -OH trong phân tử ancol bằng nguyên tử halogen.
C2H5OH + HBr → C2H5Br + H2O
- Cộng hợp hiđro halogenua hoặc halogen vào phân tử hiđrocacbon không no.
CH2=CH2 + HBr → CH3-CH2-Br
CH2=CH2 + Br2 → Br-CH2-CH2-Br
- Thế nguyên tử H của hiđrocacbon bằng nguyên tử halogen.
CH4 + Cl2 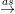 CH3Cl + HCl
CH3Cl + HCl
2. Phân loại dẫn xuất halogen
• Các dẫn xuất halogen được phân loại dựa vào bản chất của halogen, số lượng nguyên tử halogen và đặc điểm cấu tạo của hidrocacbon
• Một số loại dẫn xuất halogen thường gặp
- Dẫn xuất halogen của hiđrocacbon no, mạch hở.
- Dẫn xuất halogen của hiđrocacbon không no, mạch hở.
- Dẫn xuất halogen của hiđrocacbon thơm
• Bậc của dẫn xuất halogen bằng bậc của nguyên tử cacbon liên kết với nguyên tử halogen.
- Bậc I: 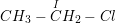 (Etyl clorua)
(Etyl clorua)
- Bậc II: 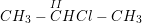 (isopropyl clorua)
(isopropyl clorua)
- Bậc III: 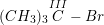 (tert-butyl bromua)
(tert-butyl bromua)
II. Tính chất vật lý của dẫn xuất halogen
• Ở điều kiện thường, một số chất có phân tử khối nhỏ (CH3Q, CH3F,...) ở trạng thái khí.
• Các dẫn xuất halogen hầu như không tan trong nước, tan tốt trong các dung môi hữu cơ như hiđrocacbon, ete,...
• Một số dẫn xuất halogen có hoạt tính sinh học cao như CF3-CHClBr (halotan: chất gây mê không độc), DDT (chất diệt côn trùng),...
III. Tính chất hóa học của dẫn xuất halogen
- Tính chất quan trọng của dẫn xuất halogen là phản ứng thế nguyên tử halogen và phản ứng tách halogenua
1. Phản ứng thế nguyên tử halogen bằng nhóm -OH
• Đun nhẹ hỗn hợp gồm etyl bromua trong dung dịch NaOH, đồng thời lắc đều. Sau một thời gian thu được hỗn hợp đồng nhất, do đã xảy ra phản ứng:
CH3-CH2-Br + NaOH(loãng) 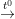 CH3-CH2-OH + NaBr
CH3-CH2-OH + NaBr
Phương trình hoá học tổng quát:
R-X + NaOH 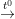 R-OH + NaX
R-OH + NaX
2. Phản ứng tách hiđro halogenua
- Đun sôi hỗn hợp gồm etyl bromua, kali hiđroxit và etanol thấy có khí không màu thoát ra.
H-CH2-CH2-Br + KOH ![small xrightarrow[t^{0}]{C_{2}H_{5}OH}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710465xvldo0aiiz_1639477948.gif) CH2=CH2 + KBr + H2O
CH2=CH2 + KBr + H2O
IV. Ứng dụng của dẫn xuất halogen
1. Làm nguyên liệu cho tổng hợp hữu cơ
a) Các dẫn xuất clo của etilen, butađien được dùng làm monome cho tổng hợp polime:
- Từ CH2=CHCl tổng hợp được poli(vinyl clorua) 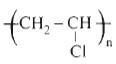 dùng làm ống dẫn, vỏ bọc dây điện, vải giả da,...
dùng làm ống dẫn, vỏ bọc dây điện, vải giả da,...
- Từ CH2=CCl−CH=CH2 tổng hợp ra 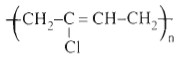 để sản xuất cao su cloropren.
để sản xuất cao su cloropren.
- Từ CF2=CF2 tổng hợp ra teflon 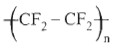 là vật liệu siêu bền,chịu nhiệt, chịu axit và kiềm, được dùng chế tạo chảo không dính, bộ phận chịu mài mòn, ...
là vật liệu siêu bền,chịu nhiệt, chịu axit và kiềm, được dùng chế tạo chảo không dính, bộ phận chịu mài mòn, ...
b) Các dẫn xuất halogen, đặc biệt là dẫn xuất monohalogen được dùng làm nguyên liệu tổng hợp các hợp chất khác như ancol, phenol, ...
2. Làm dung môi
- Clorofom, 1,2-đicloetan, cacbon tetraclorua và nhiều dẫn xuất halogen có khả năng hoà tan tốt các chất nên được dùng làm dung môi.
3. Các lĩnh vực khác
- Nhiều dẫn xuất của halogen có tác dụng trừ sâu, diệt khuẩn (2,4-D; DDT;..) tuy nhiên do độc tính cao và phân hủy chậm nên đang được thay thế bằng các chất khác an toàn và hiệu quả hơn.
- Một số chất được làm thuốc gây mê trong phẫu thuật như halotan CF3-CHClBr (chất gây mê qua đường hô hấp), etyl clorua C2H5Cl (chất gây tê cục bộ),...
V. Bài tập về dẫn xuất halogen của Hiđrocacbon
* Bài 1 trang 177 SGK Hóa 11: Gọi tên mỗi chất sau: CH3-CH2Cl, CH2=CH-CH2Cl, CHCl3. C6H5Cl. Viết phương trình hoá học của các phản ứng điều chế mỗi chất trên từ hiđrocacbon tương ứng.
° Lời giải bài 1 trang 177 SGK Hóa 11:
• Gọi tên các chất:
CH3-CH2Cl: Etyl clorua (cloetan)
CH2=CH-CH2Cl: anlyl clorua (1-cloprop-2-en)
CHCl3: Triclometan, clorofom
C6H5Cl: Clobenzen, phenyl clorua
• Cách điều chế
CH3CH3 + Cl2 ![small xrightarrow[]{askt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710467imfy39tb1f_1639477949.gif) CH3- CH2Cl + HCl
CH3- CH2Cl + HCl
CH2=CH-CH3 + Cl2 ![small small xrightarrow[]{450^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710468ntilzg0ldy_1639477949.gif) CH2 = CH- CH2Cl +HCl
CH2 = CH- CH2Cl +HCl
CH4 + 3Cl2 ![small xrightarrow[]{askt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710467imfy39tb1f_1639477949.gif) CHCl3 + 3HCl
CHCl3 + 3HCl
C6H6 + Cl2 ![small dpi{100} small small xrightarrow[]{t^{0},Fe}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710471nzerusqtpt_1639477950.gif) C6H5Cl + HCl
C6H5Cl + HCl
* Bài 2 trang 177 SGK Hóa 11: Viết phương trình hoá học của phản ứng thuỷ phân các chất sau trong dung dịch NaOH: 1,2- đicloetan; benzylclorua; antyl bromua; xiclohexyl clorua.
° Lời giải bài 2 trang 177 SGK Hóa 11:
• Phương trình phản ứng:
Cl-CH2-CH2-Cl + 2NaOH 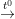 OH-CH2-CH2-OH + 2NaCl
OH-CH2-CH2-OH + 2NaCl
C6H5-CH2-Cl + NaOH 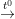 C6H5-CH2-OH + NaCl
C6H5-CH2-OH + NaCl
CH2=CH-CH2-Br + NaOH 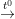 CH2=CH-CH2-OH + NaBr
CH2=CH-CH2-OH + NaBr
C6H11-Cl + NaOH 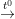 C6H11-OH + NaCl
C6H11-OH + NaCl
* Bài 3 trang 177 SGK Hóa 11: Cho nhiệt độ sôi (oC) của một số dẫn xuất halogen trong bảng dưới đây:
| X | Cl | Br | I |
| CH3-X | -24 | 5 | 42 |
| C2H5-X | 1 | 38 | 72 |
| n-C3H7-X | 47 | 71 | 102 |
| n-C4H9-X | 78 | 102 | 131 |
Nhận xét về sự biến đổi nhiệt độ sôi theo chiều tăng mạch cacbon (theo hàng dọc) và theo nguyên tử khối của halogen (hàng ngang). Giải thích sơ bộ.
° Lời giải bài 3 trang 177 SGK Hóa 11:
- Theo chiều tăng mạch cacbon (hàng dọc), nguyên từ khối tăng nhiệt độ sôi của các chất tăng dần.
- Khi nguyên tử khối tăng (theo hàng ngang), nhiệt độ sôi cùng giảm dần.
- Khi nguyên tử khối tăng cần tốn nhiều năng lượng để chuyển các phân tử hữu cơ sang trạng thái hơi nhiệt độ sôi tăng.
* Bài 4 trang 177 SGK Hóa 11: Từ axetilen, viết phương trình hoá học của các phản ứng điều chế: etyl bromua (1); 1,2-đibrometan (2); vinyl clorua (3); 1,1-đibrometan (4).
° Lời giải bài 4 trang 177 SGK Hóa 11:
(1) điều chế etyl bromua
CH≡CH + H2 ![small xrightarrow[]{t^{0},Ni}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/157871183338rgy40pup_1639477951.gif) C2H6
C2H6
CH3-CH3 + Br2 ![small xrightarrow[]{as}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578711835jug0vfmeox_1639477951.gif) CH3-CH2-Br + HBr
CH3-CH2-Br + HBr
(2) điều chế 1,2-đibrometan
CH≡CH + H2 ![small xrightarrow[]{t^{0},Pb/PbCO_{3}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/pbco_1578711836_1639477951.gif) CH2=CH2
CH2=CH2
CH2=CH2 + Br2 → CH3Br – CH3Br
(3) điều chế vinyl clorua
CH≡CH + HCl ![small xrightarrow[]{150-200^{0}C,HgCl_{2}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/15787118385q9on4igh1_1639477953.gif) CH2=CH-Cl
CH2=CH-Cl
(4) điều chế 1,1 –đibrometan
CH≡CH + HBr ![small xrightarrow[]{t^{0},xt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578711839d5kjw6fgic_1639477953.gif) CH2=CHBr
CH2=CHBr
CH2=CHBr + HBr ![small xrightarrow[]{t^{0},xt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578711839d5kjw6fgic_1639477953.gif) CH3-CHBr2
CH3-CHBr2
* Bài 5 trang 177 SGK Hóa 11: Dùng hai ống nghiệm, mỗi ống đựng 1ml một chất lỏng sau: etyl bromua (1), brombenzen (2). Thêm tiếp vào mỗi ống 1 ml dung dịch AgNO3. Đun sôi hai ống nghiệm thấy ở (1) có kết tủa vàng nhạt, trong khi đó ở ống (2) không có hiện tượng gì. Nhận xét, giải thích các hiện tượng thí nghiệm trên?
° Lời giải bài 5 trang 177 SGK Hóa 11:
- Ống (1) có phản ứng:
CH3 – CH2Br + H2O 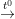 CH3- CH2OH + HBr
CH3- CH2OH + HBr
AgNO3 + HBr → AgBr↓vàng nhạt + HNO3
- Ống (2) không có phản ứng, chứng tỏ liên kết C- Br trong brombenzen rất bền
* Bài 6 trang 177 SGK Hóa 11: Khi đun nóng etyl clorua trong dung dịch chứa KOH và C2H5OH, thu được:
A. Etanol B. Etilen C. Axetilen D. Etan
° Lời giải bài 6 trang 177 SGK Hóa 11:
• Chọn đáp án: B. Etilen
CH3CH2-Cl + KOH ![small xrightarrow[t^{0}]{C_{2}H_{5}OH}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710465xvldo0aiiz_1639477948.gif) CH2=CH2 + KCl + H2O
CH2=CH2 + KCl + H2O
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo Bài 5 trang 91 SGK Hoá 11 Cánh diều
Bài 5 trang 91 SGK Hoá 11 Cánh diều Bài 4 trang 91 SGK Hoá 11 Cánh diều
Bài 4 trang 91 SGK Hoá 11 Cánh diều Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene Bài 2 trang 91 SGK Hoá 11 Cánh diều
Bài 2 trang 91 SGK Hoá 11 Cánh diều Bài 1 trang 91 SGK Hoá 11 Cánh diều
Bài 1 trang 91 SGK Hoá 11 Cánh diều Bài 6 trang 99 SGK Hoá 11 Cánh diều
Bài 6 trang 99 SGK Hoá 11 Cánh diều Bài 5 trang 99 SGK Hoá 11 Cánh diều
Bài 5 trang 99 SGK Hoá 11 Cánh diều Bài 4 trang 99 SGK Hoá 11 Cánh diều
Bài 4 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 99 SGK Hoá 11 Cánh diều
Bài 3 trang 99 SGK Hoá 11 Cánh diều Bài 2 trang 99 SGK Hoá 11 Cánh diều
Bài 2 trang 99 SGK Hoá 11 Cánh diều Bài 1 trang 99 SGK Hoá 11 Cánh diều
Bài 1 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học Bài 2 trang 106 SGK Hoá 11 Cánh diều
Bài 2 trang 106 SGK Hoá 11 Cánh diều Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen Bài 5 trang 71 SGK Hoá 11 Cánh diều
Bài 5 trang 71 SGK Hoá 11 Cánh diều Bài 4 trang 71 SGK Hoá 11 Cánh diều
Bài 4 trang 71 SGK Hoá 11 Cánh diều Bài 3 trang 71 SGK Hoá 11 Cánh diều
Bài 3 trang 71 SGK Hoá 11 Cánh diều Bài 2 trang 71 SGK Hoá 11 Cánh diều
Bài 2 trang 71 SGK Hoá 11 Cánh diều Bài 1 trang 71 SGK Hoá 11 Cánh diều
Bài 1 trang 71 SGK Hoá 11 Cánh diều Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
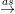 CH3Cl + HCl
CH3Cl + HCl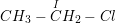 (Etyl clorua)
(Etyl clorua)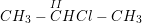 (isopropyl clorua)
(isopropyl clorua)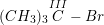 (tert-butyl bromua)
(tert-butyl bromua)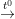 CH3-CH2-OH + NaBr
CH3-CH2-OH + NaBr![small xrightarrow[t^{0}]{C_{2}H_{5}OH}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710465xvldo0aiiz_1639477948.gif) CH2=CH2 + KBr + H2O
CH2=CH2 + KBr + H2O![small xrightarrow[]{askt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710467imfy39tb1f_1639477949.gif) CH3- CH2Cl + HCl
CH3- CH2Cl + HCl![small small xrightarrow[]{450^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710468ntilzg0ldy_1639477949.gif) CH2 = CH- CH2Cl +HCl
CH2 = CH- CH2Cl +HCl![small dpi{100} small small xrightarrow[]{t^{0},Fe}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578710471nzerusqtpt_1639477950.gif) C6H5Cl + HCl
C6H5Cl + HCl![small xrightarrow[]{t^{0},Ni}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/157871183338rgy40pup_1639477951.gif) C2H6
C2H6![small xrightarrow[]{as}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578711835jug0vfmeox_1639477951.gif) CH3-CH2-Br + HBr
CH3-CH2-Br + HBr![small xrightarrow[]{t^{0},Pb/PbCO_{3}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/pbco_1578711836_1639477951.gif) CH2=CH2
CH2=CH2![small xrightarrow[]{150-200^{0}C,HgCl_{2}}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/15787118385q9on4igh1_1639477953.gif) CH2=CH-Cl
CH2=CH-Cl![small xrightarrow[]{t^{0},xt}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578711839d5kjw6fgic_1639477953.gif) CH2=CHBr
CH2=CHBr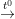 CH3- CH2OH + HBr
CH3- CH2OH + HBr











































