Giải bài 8 trang 38 SGK Hoá 11: Amoniac và muối Amoni
09:30:48Cập nhật: 07/10/2022
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,00 gram NH3...
Hy vọng với lời giải bài 8 trang 38 SGK Hoá 11: Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,00 gram NH3...? ở trên đã giúp các em hiểu và nắm vững phần kiến thức này. Mọi góp ý và thắc mắc các em hãy để lại nhận xét dưới bài viết để Hay Học Hỏi ghi nhận và hỗ trợ, chúc các em học tốt.
• Xem các bài tập Hoá 11 cùng chuyên mục
> Bài 2 trang 37 SGK Hóa 11: Hoàn thành sơ đồ chuyển hóa sau và viết các phương trình hóa học:...
Đánh giá & nhận xét
Tin liên quan
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo Bài 5 trang 91 SGK Hoá 11 Cánh diều
Bài 5 trang 91 SGK Hoá 11 Cánh diều Bài 4 trang 91 SGK Hoá 11 Cánh diều
Bài 4 trang 91 SGK Hoá 11 Cánh diều Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene
Bài 3 trang 91 SGK Hoá 11 Cánh diều: Nhận Biết Ethane, Ethylene, Acetylene Bài 2 trang 91 SGK Hoá 11 Cánh diều
Bài 2 trang 91 SGK Hoá 11 Cánh diều Bài 1 trang 91 SGK Hoá 11 Cánh diều
Bài 1 trang 91 SGK Hoá 11 Cánh diều Bài 6 trang 99 SGK Hoá 11 Cánh diều
Bài 6 trang 99 SGK Hoá 11 Cánh diều Bài 5 trang 99 SGK Hoá 11 Cánh diều
Bài 5 trang 99 SGK Hoá 11 Cánh diều Bài 4 trang 99 SGK Hoá 11 Cánh diều
Bài 4 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 99 SGK Hoá 11 Cánh diều
Bài 3 trang 99 SGK Hoá 11 Cánh diều Bài 2 trang 99 SGK Hoá 11 Cánh diều
Bài 2 trang 99 SGK Hoá 11 Cánh diều Bài 1 trang 99 SGK Hoá 11 Cánh diều
Bài 1 trang 99 SGK Hoá 11 Cánh diều Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học
Bài 3 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen & Nhiệt Hóa Học Bài 2 trang 106 SGK Hoá 11 Cánh diều
Bài 2 trang 106 SGK Hoá 11 Cánh diều Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen
Bài 1 trang 106 SGK Hoá 11 Cánh diều: Dẫn Xuất Halogen Bài 5 trang 71 SGK Hoá 11 Cánh diều
Bài 5 trang 71 SGK Hoá 11 Cánh diều Bài 4 trang 71 SGK Hoá 11 Cánh diều
Bài 4 trang 71 SGK Hoá 11 Cánh diều Bài 3 trang 71 SGK Hoá 11 Cánh diều
Bài 3 trang 71 SGK Hoá 11 Cánh diều Bài 2 trang 71 SGK Hoá 11 Cánh diều
Bài 2 trang 71 SGK Hoá 11 Cánh diều Bài 1 trang 71 SGK Hoá 11 Cánh diều
Bài 1 trang 71 SGK Hoá 11 Cánh diều Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 4 trang 71 Hóa 11 Cánh Diều SGK Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 5 trang 71 Hóa 11 Cánh Diều SGK Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Giải bài 3 trang 71 Hóa 11 Cánh Diều SGK
Tin mới
Tin cùng chuyên mục
Tin xem nhiều nhất

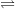 2NH3 (t0,xt,p)
2NH3 (t0,xt,p)











































