Giải bài 5 trang 29 Hoá 11 SGK Chân trời sáng tạo
Chào các em! Hôm nay, chúng ta sẽ cùng nhau giải chi tiết Bài 5 trang 29 SGK Hóa 11 thuộc bộ sách Chân trời sáng tạo. Bài toán này giúp chúng ta ôn tập và củng cố kiến thức về tính chất hóa học của muối ammonium, cụ thể là các phản ứng của amoni sunfat (NH4)2SO4 với các dung dịch khác.
Qua bài tập này, các em đã rèn luyện kỹ năng viết phương trình hóa học và xác định điều kiện xảy ra phản ứng trao đổi ion. Các phản ứng của muối ammonium rất đa dạng và thường tạo ra khí amoniac. Khi ion sunfat có mặt, phản ứng với các ion kim loại như bari sẽ tạo ra kết tủa đặc trưng. Nắm vững các phản ứng này sẽ giúp các em giải quyết các bài toán nhận biết và tách chất hiệu quả.
• Xem thêm:
Bài 1 trang 29 Hoá 11 SGK Chân trời sáng tạo: Liên kết hóa học trong phân tử NH3 là liên kết...
Đánh giá & nhận xét
 Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 107 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 98 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 56 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 51 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 132 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 39 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 39 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 39 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 39 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 39 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 39 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 39 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 39 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 34 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 34 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 34 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 34 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 34 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 34 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 29 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 29 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 29 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 29 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 29 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 29 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 29 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 29 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 23 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 23 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 23 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 23 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 23 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 23 Hoá 11 SGK Chân trời sáng tạo Giải bài 5 trang 19 Hoá 11 SGK Chân trời sáng tạo
Giải bài 5 trang 19 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 19 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 19 Hoá 11 SGK Chân trời sáng tạo Giải bài 3 trang 19 Hoá 11 SGK Chân trời sáng tạo
Giải bài 3 trang 19 Hoá 11 SGK Chân trời sáng tạo Giải bài 2 trang 19 Hoá 11 SGK Chân trời sáng tạo
Giải bài 2 trang 19 Hoá 11 SGK Chân trời sáng tạo Giải bài 1 trang 19 Hoá 11 SGK Chân trời sáng tạo
Giải bài 1 trang 19 Hoá 11 SGK Chân trời sáng tạo Giải Hóa 11 trang 23 SGK Chân trời sáng tạo
Giải Hóa 11 trang 23 SGK Chân trời sáng tạo Giải bài 5 trang 11 Hoá 11 SGK Chân trời sáng tạo
Giải bài 5 trang 11 Hoá 11 SGK Chân trời sáng tạo Giải bài 4 trang 11 Hoá 11 SGK Chân trời sáng tạo
Giải bài 4 trang 11 Hoá 11 SGK Chân trời sáng tạo

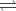 2NH3(g)
2NH3(g) 











































