Giải bài 8 trang 111 SGK Hoá 12: Tính chất hóa học của kim loại kiềm, hợp chất của kim loại kiềm
20:09:22Cập nhật: 19/10/2022
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước...
Hy vọng với lời giải bài 8 trang 111 SGK Hoá 12 ở trên đã giúp các em hiểu và nắm vững phần kiến thức này. Mọi góp ý và thắc mắc các em hãy để lại nhận xét dưới bài viết để Hay Học Hỏi ghi nhận và hỗ trợ, chúc các em học tốt.
• Xem các bài tập Hoá 12 cùng chuyên mục
> Bài 1 trang 111 SGK Hóa 12: Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm là:...
> Bài 4 trang 111 SGK Hóa 12: Trong các muối sau, muối nào dễ bị nhiệt phân:...
Đánh giá & nhận xét
Tin liên quan
 Phương pháp giải các dạng bài tập về Sắt Fe, hỗn hợp và hợp chất của Sắt - hóa lớp 12
Phương pháp giải các dạng bài tập về Sắt Fe, hỗn hợp và hợp chất của Sắt - hóa lớp 12 Giải bài 4 trang 49 Hóa 12 Chân trời sáng tạo SGK
Giải bài 4 trang 49 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 49 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 49 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 49 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 49 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 49 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 49 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 80 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 80 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 80 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 80 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 80 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 80 Hóa 12 Chân trời sáng tạo SGK Giải bài 4 trang 109 Hóa 12 Chân trời sáng tạo SGK
Giải bài 4 trang 109 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 109 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 109 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 109 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 109 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 109 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 109 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 54 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 54 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 54 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 54 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 114 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 114 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 114 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 114 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 114 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 114 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 90 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 90 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 90 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 90 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 90 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 90 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 84 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 84 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 84 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 84 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 84 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 84 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 119 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 119 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 119 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 119 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 119 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 119 Hóa 12 Chân trời sáng tạo SGK Giải bài 3 trang 44 Hóa 12 Chân trời sáng tạo SGK
Giải bài 3 trang 44 Hóa 12 Chân trời sáng tạo SGK Giải bài 2 trang 44 Hóa 12 Chân trời sáng tạo SGK
Giải bài 2 trang 44 Hóa 12 Chân trời sáng tạo SGK Giải bài 1 trang 44 Hóa 12 Chân trời sáng tạo SGK
Giải bài 1 trang 44 Hóa 12 Chân trời sáng tạo SGK Giải bài 9 trang 12 Hóa 12 Kết nối tri thức SGK
Giải bài 9 trang 12 Hóa 12 Kết nối tri thức SGK Giải bài 8 trang 11 Hóa 12 Kết nối tri thức SGK
Giải bài 8 trang 11 Hóa 12 Kết nối tri thức SGK Giải bài 7 trang 9 Hóa 12 Kết nối tri thức SGK
Giải bài 7 trang 9 Hóa 12 Kết nối tri thức SGK Giải bài 6 trang 9 Hóa 12 Kết nối tri thức SGK
Giải bài 6 trang 9 Hóa 12 Kết nối tri thức SGK Giải bài 5 trang 9 Hóa 12 Kết nối tri thức SGK
Giải bài 5 trang 9 Hóa 12 Kết nối tri thức SGK Giải bài 4 trang 9 Hóa 12 Kết nối tri thức SGK
Giải bài 4 trang 9 Hóa 12 Kết nối tri thức SGK Giải bài 3 trang 8 Hóa 12 Kết nối tri thức SGK
Giải bài 3 trang 8 Hóa 12 Kết nối tri thức SGK Giải bài 2 trang 7 Hóa 12 Kết nối tri thức SGK
Giải bài 2 trang 7 Hóa 12 Kết nối tri thức SGK Giải bài 1 trang 7 Hóa 12 Kết nối tri thức SGK
Giải bài 1 trang 7 Hóa 12 Kết nối tri thức SGK Giải bài 4 trang 38 Hóa 12 Chân trời sáng tạo SGK
Giải bài 4 trang 38 Hóa 12 Chân trời sáng tạo SGK
Tin mới
Tin cùng chuyên mục
Tin xem nhiều nhất

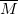
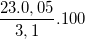 % = 37,1%
% = 37,1%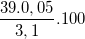 % = 62,9%
% = 62,9%










































