Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo
Liên kết cộng hóa trị không chỉ được giải thích qua việc góp chung electron mà còn được mô tả một cách trực quan thông qua thuyết lượng tử về sự xen phủ các orbital nguyên tử (AO). Đối với phân tử chlorine ($Cl_2$), sự xen phủ các orbital p là yếu tố then chốt tạo nên liên kết bền vững. Việc hiểu rõ mô hình xen phủ này sẽ giúp các em nắm vững bản chất của liên kết đơn ($\sigma$).
Qua lời giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo, các em cần nhớ:
Xen phủ trục (head-to-head overlap): Luôn tạo ra liên kết $\sigma$.
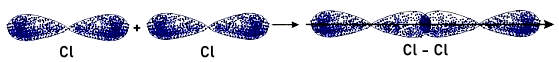
Đặc điểm liên kết trong $Cl_2$: Là liên kết cộng hóa trị không phân cực, hình thành từ sự xen phủ $p-p$.
Ghi nhớ: Mọi liên kết đơn trong các phân tử như $H_2, Cl_2, HCl$ đều là liên kết $\sigma$ được hình thành từ sự xen phủ trục của các AO.
• Xem thêm:
Đánh giá & nhận xét
 Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí
Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat
Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide
Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên
Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen
Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo
























![[Đầy đủ] Bài tập về đồ thị hàm số bậc hai, các...](https://hayhochoi.vn/thumbs_size/2020_12/[180x135-cr]1608189815ixfiqbkeca.jpg)




















