Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo
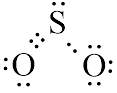
Trong thế giới hóa học, bên cạnh việc góp chung electron công bằng, còn có một hình thức liên kết đặc biệt nơi một nguyên tử "hào phóng" cung cấp cả cặp electron cho nguyên tử khác dùng chung. Đó chính là liên kết cho – nhận. Phân tử Sulfur dioxide ($SO_2$) là ví dụ kinh điển để các em tìm hiểu về cơ chế này cũng như cách viết công thức cấu tạo tương ứng.
Qua lời giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo, các em cần nhớ:
Liên kết cho – nhận: Là liên kết cộng hóa trị mà cặp electron dùng chung chỉ do một nguyên tử đóng góp.
Điều kiện: Nguyên tử cho phải còn cặp electron tự do và nguyên tử nhận phải còn ô trống hoặc thiếu electron để đạt cấu hình bền vững.
Ký hiệu: Sử dụng mũi tên ($\rightarrow$) để phân biệt với liên kết cộng hóa trị thông thường.
• Xem thêm:
Đánh giá & nhận xét
 Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí
Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat
Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide
Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên
Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen
Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo























![[Đầy đủ] Bài tập về đồ thị hàm số bậc hai, các...](https://hayhochoi.vn/thumbs_size/2020_12/[180x135-cr]1608189815ixfiqbkeca.jpg)




















