Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo
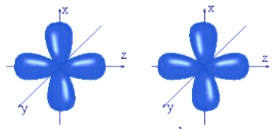
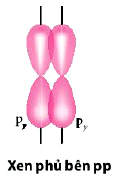
Trong lý thuyết liên kết hóa học, việc các orbital nguyên tử (AO) xen phủ với nhau như thế nào sẽ quyết định loại liên kết và độ bền của phân tử đó. Đối với các orbital p (có hình số 8 nổi), tùy thuộc vào định hướng không gian mà chúng có thể tạo ra liên kết $\sigma$ hoặc liên kết $\pi$. Hiểu rõ quy luật này là nền tảng để các em giải thích cấu trúc của các phân tử có liên kết bội như $O_2, N_2$ hay các hợp chất hữu cơ.
Qua lời giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo, các em cần nhớ:
Nguyên tắc: Một liên kết đơn luôn là liên kết $\sigma$. Liên kết đôi gồm 1 $\sigma$ và 1 $\pi$. Liên kết ba gồm 1 $\sigma$ và 2 $\pi$.
Độ bền: Liên kết $\sigma$ bền hơn liên kết $\pi$ do vùng xen phủ lớn hơn.
Ghi nhớ: Các AO $p_z$ thường được quy ước nằm trên trục liên kết để tạo liên kết $\sigma$, trong khi $p_x, p_y$ sẽ tạo liên kết $\pi$.
• Xem thêm:
Đánh giá & nhận xét
 Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí
Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat
Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide
Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên
Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen
Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 34 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 25 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 19 SGK Hoá 10 Chân trời sáng tạo




















![[Tổng hợp đầy đủ] Giới hạn của hàm số, cách tính và bài tập Toán 11](https://hayhochoi.vn/thumbs_size/news/2018_09/[180x135-cr]gioi-han-cua-ham-so.jpg)



![[Đầy đủ] Bài tập về đồ thị hàm số bậc hai, các...](https://hayhochoi.vn/thumbs_size/2020_12/[180x135-cr]1608189815ixfiqbkeca.jpg)




















