Bảng Tính Tan Trong Nước Của Các Axit, Bazơ, Muối - Hỏi đáp Hóa học 8
Trong chương trình Hóa học lớp 8, bảng tính tan là công cụ hỗ trợ đắc lực giúp các em xác định được trạng thái của chất (kết tủa, bay hơi hay hòa tan) trong các phản ứng hóa học.
Vậy cụ thể bảng tính tan trong nước của một số chất này như thế nào? Câu trả lời đầy đủ, dễ hiểu sẽ có trong nội dung bài viết này để các em tham khảo.
1. Bảng tính tan trong nước của một số chất lớp 8
Dưới đây là bảng chi tiết về tính tan của các hợp chất khi kết hợp giữa các kim loại (hoặc Hydrogen) với nhóm Hydroxide và các gốc Acid:
| Nhóm hydroxide và gốc acid | H (I) | K (I) | Na (I) | Ag (I) | Mg (II) | Ca (II) | Ba (II) | Zn (II) | Hg (II) | Pb (II) | Cu (II) | Fe (II) | Fe (III) | Al (III) |
| -OH | T | T | – | K | I | T | K | – | K | K | K | K | K | |
| -Cl | T/B | T | T | K | T | T | T | T | T | I | T | T | T | T |
| -NO₃ | T/B | T | T | T | T | T | T | T | T | T | T | T | T | T |
| CH₃COO- | T/B | T | T | T | T | T | T | T | T | T | T | T | – | I |
| =S | T/B | T | T | K | – | T | T | K | K | K | K | K | K | – |
| =SO₃ | T/B | T | T | K | K | K | K | K | K | K | K | K | – | – |
| =SO₄ | T/Kb | T | T | I | T | I | K | T | – | K | T | T | T | T |
| =CO₃ | T/B | T | T | K | K | K | K | K | – | K | – | K | – | – |
| =SiO₃ | K/Kb | T | T | – | K | K | K | K | – | K | – | K | K | K |
| ≡PO₄ | T/Kb | T | T | K | K | K | K | K | K | K | K | K | K | K |
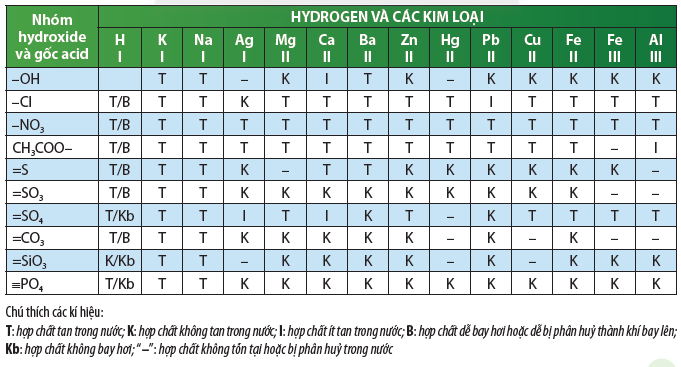 Bảng tính tan trong nước của một số chất lớp 8.
Bảng tính tan trong nước của một số chất lớp 8.
2. Giải thích các ký hiệu trong bảng tính tan
Để sử dụng bảng tính tan một cách hiệu quả, các em cần ghi nhớ ý nghĩa của các ký hiệu sau:
-
T: Hợp chất tan trong nước.
-
K: Hợp chất không tan (kết tủa) trong nước.
-
I: Hợp chất ít tan trong nước.
-
B: Hợp chất dễ bay hơi hoặc dễ bị phân hủy thành khí bay lên.
-
Kb: Hợp chất không bay hơi.
-
"–": Hợp chất không tồn tại hoặc bị phân hủy trong nước.
3. Mẹo ghi nhớ tính tan nhanh nhất (Bài ca tính tan)
Thay vì học thuộc lòng từng ô trong bảng, các em có thể ghi nhớ nhanh qua các quy tắc rút gọn sau:
Quy tắc về muối:
-
Tất cả các muối Nitrat (-NO₃) và muối của kim loại kiềm (Li, Na, K) đều TAN.
-
Hầu hết các muối Clorua (-Cl) và Sunfat (=SO₄) đều TAN (trừ $AgCl$ kết tủa trắng, $BaSO_4$ và $PbSO_4$ kết tủa trắng).
-
Hầu hết các muối Cacbonat (=CO₃), Sunfit (=SO₃) và Photphat (≡PO₄) đều KHÔNG TAN (trừ muối của $Na, K, Li$).
Quy tắc về Bazơ (nhóm -OH):
-
Các bazơ của kim loại kiềm và kiềm thổ (K, Na, Ba, Ca, Li) là bazơ TAN (Kiềm).
-
Các bazơ còn lại đều KHÔNG TAN (kết tủa màu đặc trưng như $Cu(OH)_2$ xanh, $Fe(OH)_3$ nâu đỏ...).
Xem thêm: Công thức tính độ tan S của một chất và bài tập áp dụng
4. Tại sao cần thuộc bảng tính tan?
Việc nắm vững tính tan của các chất giúp học sinh lớp 8:
-
Viết đúng phương trình phản ứng: Biết được sản phẩm có tạo thành kết tủa hay khí hay không để thỏa mãn điều kiện phản ứng trao đổi.
-
Nhận biết các chất: Dựa vào màu sắc và tính tan để phân biệt các lọ mất nhãn.
-
Làm bài tập định lượng: Tính toán khối lượng kết tủa hoặc nồng độ dung dịch sau phản ứng.
Hy vọng bảng tính tan lớp 8 và những hướng dẫn chi tiết trên đây sẽ giúp các em tự tin hơn khi học tập bộ môn Hóa học. Hãy truy cập hayhochoi.vn mỗi ngày để cập nhật những kiến thức bổ ích và lời giải bài tập SGK chi tiết nhé!
Đánh giá & nhận xét
-
 Bài tập luyện tập về điều chế HIDRO và phản ứng thế, phản ứng OXI HÓA KHỬ - Hóa 8 bài 34
Bài tập luyện tập về điều chế HIDRO và phản ứng thế, phản ứng OXI HÓA KHỬ - Hóa 8 bài 34
-
 Tỉ khối là gì, công thức và cách tính tỉ khối của chất khí, hỗn hợp khí - hoá 8 bài 20
Tỉ khối là gì, công thức và cách tính tỉ khối của chất khí, hỗn hợp khí - hoá 8 bài 20
-
 Cách lập phương trình hóa học, ý nghĩa của phương trình hóa học và Bài tập - Hóa 8 bài 16
Cách lập phương trình hóa học, ý nghĩa của phương trình hóa học và Bài tập - Hóa 8 bài 16
-
 Hóa trị là gì? Quy tắc, cách tính hóa trị và bảng hóa trị nguyên tố (Hóa 8 bài 10)
Hóa trị là gì? Quy tắc, cách tính hóa trị và bảng hóa trị nguyên tố (Hóa 8 bài 10)
-
 Màu sắc một số chất kết tủa và dung dịch thường gặp trong hóa học
Màu sắc một số chất kết tủa và dung dịch thường gặp trong hóa học
-
 Công thức tính độ tan S (lớp 8) của một chất trong nước? Hỏi đáp Hóa học 8
Công thức tính độ tan S (lớp 8) của một chất trong nước? Hỏi đáp Hóa học 8
-
 Bảng hóa trị của các nguyên tố hóa học và Bảng hóa trị của một số nhóm nguyên tử - Hóa lớp 8
Bảng hóa trị của các nguyên tố hóa học và Bảng hóa trị của một số nhóm nguyên tử - Hóa lớp 8
-
 Giải bài 1 trang 79 SGK Hoá 8: Luyện tập mol, khối lượng mol, thể tích mol, tỉ khối chất khí
Giải bài 1 trang 79 SGK Hoá 8: Luyện tập mol, khối lượng mol, thể tích mol, tỉ khối chất khí
-
 Giải bài 1 trang 100 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 1 trang 100 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 2 trang 100 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 2 trang 100 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 3 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 3 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 4 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 4 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 5 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 5 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 6 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 6 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 7 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 7 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 8 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
Giải bài 8 trang 101 SGK Hoá 8: Luyện tập điều chế Oxi, phân loại Oxít, Sự Oxi hoá, phản ứng phân huỷ, phản ứng hoá hợp
-
 Giải bài 1 trang 131 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
Giải bài 1 trang 131 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
-
 Giải bài 2 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
Giải bài 2 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
-
 Giải bài 3 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
Giải bài 3 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
-
 Giải bài 4 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
Giải bài 4 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
-
 Giải bài 5 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
Giải bài 5 trang 132 SGK Hoá 8: Luyện tập tính chất của nước, định nghĩa, phân loại, cách gọi tên Axit, Bazơ, Muối
-
 Giải bài 1 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
Giải bài 1 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
-
 Giải bài 2 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
Giải bài 2 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
-
 Giải bài 3 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
Giải bài 3 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
-
 Giải bài 4 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
Giải bài 4 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
-
 Giải bài 5 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
Giải bài 5 trang 149 SGK Hoá 8: Cách pha chế, pha loãng một dung dịch theo nồng độ cho trước
-
 Giải bài 1 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 1 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Giải bài 2 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 2 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Giải bài 3 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 3 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Giải bài 6 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 6 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Giải bài 5 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 5 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Giải bài 4 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
Giải bài 4 trang 151 SGK Hoá 8: Luyện tập Công thức tính nồng độ phần trăm, nồng độ mol, cách pha chế dung dịch
-
 Nồng độ Mol, Nồng độ phần trăm của dung dịch: Bài tập luyện tập - Hóa 8 bài 44
Nồng độ Mol, Nồng độ phần trăm của dung dịch: Bài tập luyện tập - Hóa 8 bài 44
-
 Cách Pha chế dung dịch theo nồng đồ cho trước và Cách tính để pha loãng dung dịch - Hóa 8 bài 43
Cách Pha chế dung dịch theo nồng đồ cho trước và Cách tính để pha loãng dung dịch - Hóa 8 bài 43
-
 Axit, Bazơ, Muối và Nước: Bài tập luyện tập về Axit Bazơ Muối - Hóa 8 bài 38
Axit, Bazơ, Muối và Nước: Bài tập luyện tập về Axit Bazơ Muối - Hóa 8 bài 38
-
 Bài tập luyện tập về Oxi, Oxit, Sự Oxi hóa, Phản ứng hóa hợp và phản ứng phân hủy - Hóa 8 bài 29
Bài tập luyện tập về Oxi, Oxit, Sự Oxi hóa, Phản ứng hóa hợp và phản ứng phân hủy - Hóa 8 bài 29
-
 Giải bài 4 trang 75 SGK Hoá 8: Cách tính theo phương trình hoá học
Giải bài 4 trang 75 SGK Hoá 8: Cách tính theo phương trình hoá học
-
 Giải bài 2 trang 60 SGK Hoá 8: Luyện tập phản ứng hoá học, phương trình hoá học, định luật bảo toàn khối lượng
Giải bài 2 trang 60 SGK Hoá 8: Luyện tập phản ứng hoá học, phương trình hoá học, định luật bảo toàn khối lượng
-
 Giải bài 1 trang 60 SGK Hoá 8: Luyện tập phản ứng hoá học, phương trình hoá học, định luật bảo toàn khối lượng
Giải bài 1 trang 60 SGK Hoá 8: Luyện tập phản ứng hoá học, phương trình hoá học, định luật bảo toàn khối lượng


















































