Tính chất hoá học của axit Clohidric HCl, Hiđro clorua và muối Clorua - hoá 10 bài 23
Axit Clo hidric HCl là chất lỏng không màu, dễ bay hơi trong khi đó Hiđro clorua (HCl) là chất khí, không màu, mùi xốc tan nhiều trong nước tạo thành dung dịch axit mạnh HCl.
Lời giải bài 7 trang 106 sgk hóa 10:
a) Theo bài ra, ta có nAgNO3 = 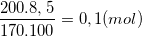
- Phương trình phản ứng:
HCl + AgNO3 → AgCl↓ + HNO3
- Theo PTPƯ thì: nHCl = nAgCl = 0,1 (mol)
⇒CM (HCl) = n/V = 0,1/0,15 = 0,667 (mol/l).
b) Theo bài ra ta có, nCO2 = V/22,4 = 2,24/22,4 = 0,1 (mol)
- Phương trình phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
- Theo PTPƯ: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
⇒ C%(HCl) = (mct/mdd).100% = (3,65/50).100% = 7,3%
Hy vọng với bài viết hệ thống lại kiến thức về tính chất hoá học của Axit Clo hidric (HCl), Hiđro clorua và muối Clorua một cách chi tiết ở trên sẽ hữu ích cho các em. Mọi thắc mắc các em hãy để lại bình luận dưới bài viết để được hỗ trợ, nếu thấy bài viết hay thì chia sẻ với bạn bè nhé, chúc các em học tập tốt.
¤ Xem thêm các bài viết khác tại:
Đánh giá & nhận xét

















 Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí
Giải bài 3 trang 119 SGK Hoá 10 Chân trời sáng tạo: Cách pha chế nước muối sinh lí Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat
Giải bài 2 trang 119 SGK Hoá 10 Chân trời sáng tạo: Điều chế Hydrogen Halide bằng phương pháp Sunfat Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide
Giải bài 1 trang 119 SGK Hoá 10 Chân trời sáng tạo: Phản Ứng Của Hydrogen Halide Và Muối Halide Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 113 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên
Giải bài 2 trang 113 SGK Hoá 10 Chân trời sáng tạo: Sự tồn tại của Halogen trong tự nhiên Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen
Giải bài 1 trang 113 SGK Hoá 10 Chân trời sáng tạo: Tính Chất Hóa Học Của Halogen Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 8 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 7 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 6 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 66 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 71 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 51 SGK Hoá 10 Chân trời sáng tạo Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 5 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 4 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo
Giải bài 1 trang 58 SGK Hoá 10 Chân trời sáng tạo Giải Hóa học 10 trang 20 - Kết nối tri thức
Giải Hóa học 10 trang 20 - Kết nối tri thức Giải Hóa học 10 trang 18 - Kết nối tri thức
Giải Hóa học 10 trang 18 - Kết nối tri thức Giải Hóa học 10 trang 17 - Kết nối tri thức
Giải Hóa học 10 trang 17 - Kết nối tri thức Giải Hóa học 10 trang 16 - Kết nối tri thức
Giải Hóa học 10 trang 16 - Kết nối tri thức Giải Hóa học 10 trang 15 - Kết nối tri thức
Giải Hóa học 10 trang 15 - Kết nối tri thức Giải Hóa học 10 trang 14 - Kết nối tri thức
Giải Hóa học 10 trang 14 - Kết nối tri thức Giải Hóa học 10 trang 13 - Kết nối tri thức
Giải Hóa học 10 trang 13 - Kết nối tri thức Giải Hóa học 10 trang 8 - Kết nối tri thức
Giải Hóa học 10 trang 8 - Kết nối tri thức Giải Hóa học 10 trang 7 - Kết nối tri thức
Giải Hóa học 10 trang 7 - Kết nối tri thức Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 3 trang 42 SGK Hoá 10 Chân trời sáng tạo Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo
Giải bài 2 trang 42 SGK Hoá 10 Chân trời sáng tạo






![small xrightarrow[]{<250^{0}C}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/1578358347w4h5z72oaf_1639446302.gif) NaHSO4 + HCl
NaHSO4 + HCl![small xrightarrow[]{>400^{0}C}](https://hayhochoi.vn/uploads/news/wyswyg/2021_12/157835834840o18c37hy_1639446302.gif) Na2SO4 + 2HCl
Na2SO4 + 2HCl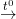 Na2SO4 + 2HCl
Na2SO4 + 2HCl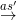 2HCl.
2HCl.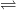 HCl + HClO
HCl + HClO











































