Tính chất hóa học các loại hợp chất vô cơ, cách phân loại các hợp chất vô cơ và bài tập luyện tập - Hóa 9 bài 13
Cách phân loại các loại hợp chất vô cơ như thế nào? Tính chất hóa học của các loại hợp chất vô cơ là gì? các em cũng đã được học ở những bài trước.
Bài viết này nhằm củng cố các kiến thức đã học về cách phân loại và tính chất hóa học của các loại hợp chất vô cơ và giải một số bài tập vận dụng.
I. Kiến thức cần nhớ về các loại hợp chất vô cơ
1. Cách phân loại các hợp chất vô cơ
• Bảng dưới đây cho chúng ta biết về hệ thống phân loại các hợp chất vô cơ:
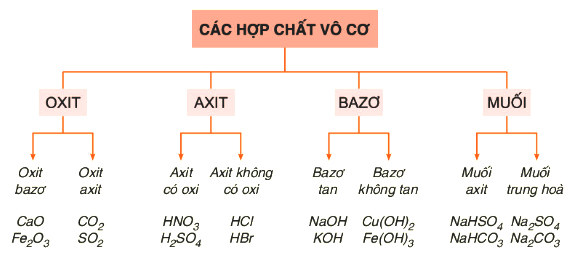 Bảng phân loại các hợp chất vô cơ
Bảng phân loại các hợp chất vô cơ
2. Tính chất hóa học của các loại hợp chất vô cơ
• Tính chất hóa học của các hợp chất vô cơ được tóm tắt bằng sơ đồ sau:
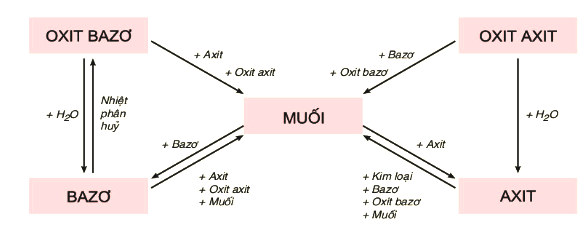 Tính chất hóa học của các hợp chất vô cơ
Tính chất hóa học của các hợp chất vô cơ
II. Bài tập luyên tập các loại hợp chất vô cơ
* Bài 1 trang 43 SGK Hóa 9: Căn cứ vào sơ đồ biểu thị những tính chất hóa học của các hợp chất vô cơ:
1. Oxit
a) Oxit bazơ + ... → bazơ
b) Oxit bazơ + ... → muối + nước
c) Oxit axit + ... → axit
d) Oxit axit + ... → muối + nước
2. Bazơ
a) Bazơ + ... → muối + nước
b) Bazơ + ... → muối + nước
c) Bazơ + ... → muối + bazơ
d) Bazơ oxit bazơ + nước
e) Oxit axit + oxit bazơ → ...
3. Axit
a) Axit + ... → muối + hiđro
b) Axit + ... → muối + nước
c) Axit + ... → muối + nước
d) Axit + ... → muối + axit
4. Muối
a) Muối + ... → axit + muối
b) Muối + ... → muối + bazơ
c) Muối + ... → muối + muối
d) Muối + ... → muối + kim loại
e) Muối ... + ...
>> Giải bài 1 trang 43 SGK Hóa 9
* Bài 2 trang 43 SGK Hóa 9: Để một mẩu natri hiđroxit trên tấm kính trong không khí, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn thấy có khí thoát ra, khí này làm đục nước vôi trong. Chất rắn màu trắng là sản phẩm phản ứng của natri hiđroxit với:
a) Oxit trong không khí.
b) Hơi nước trong không khí.
c) Cacbon đioxit và oxi trong không khí.
d) Cacbon đioxit và hơi nước trong không khí.
e) Cacbon đioxit trong không khí.
Giải thích và viết phương trình hóa học minh họa.
>> Giải bài 2 trang 43 SGK Hóa 9
* Bài 3 trang 43 SGK Hóa 9: Trộn một dung dịch có hòa tan 0,2 mol CuCl2 với một dung dịch có hòa tan 20g NaOH. Lọc hỗn hợp các chất sau phản ứng, được kết tủa và nước lọc. Nung kết tủa đến khi khối lượng không đổi.
a) Viết các phương trình hóa học.
b) Tính khối lượng chất rắn thu được sau khi nung.
c) Tính khối lượng các chất có trong nước lọc.
Hy vọng với bài viết Tính chất hóa học các loại hợp chất vô cơ, cách phân loại các hợp chất vô cơ và bài tập luyện tập Hóa lớp 9 bài 13 ở trên giúp các em giải các bài tập dạng này một cách dễ dàng. Mọi góp ý và thắc mắc các em hãy để lại nhận xét dưới bài viết để hayhochoi ghi nhận và hỗ trợ, chúc các em học tốt.
Đánh giá & nhận xét
-
 Tính chất hoá học của Oxide, Acid, Base và Muối - Hoá lớp 9
Tính chất hoá học của Oxide, Acid, Base và Muối - Hoá lớp 9
-
 Giải KHTN 9 trang 134 Chân trời sáng tạo SGK
Giải KHTN 9 trang 134 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 132 Chân trời sáng tạo SGK
Giải KHTN 9 trang 132 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 131 Chân trời sáng tạo SGK
Giải KHTN 9 trang 131 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 130 Chân trời sáng tạo SGK
Giải KHTN 9 trang 130 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 129 Chân trời sáng tạo SGK
Giải KHTN 9 trang 129 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 128 Chân trời sáng tạo SGK
Giải KHTN 9 trang 128 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 127 Chân trời sáng tạo SGK
Giải KHTN 9 trang 127 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 126 Chân trời sáng tạo SGK
Giải KHTN 9 trang 126 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 125 Chân trời sáng tạo SGK
Giải KHTN 9 trang 125 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 124 Chân trời sáng tạo SGK
Giải KHTN 9 trang 124 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 123 Chân trời sáng tạo SGK
Giải KHTN 9 trang 123 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 122 Chân trời sáng tạo SGK
Giải KHTN 9 trang 122 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 121 Chân trời sáng tạo SGK
Giải KHTN 9 trang 121 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 120 Chân trời sáng tạo SGK
Giải KHTN 9 trang 120 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 119 Chân trời sáng tạo SGK
Giải KHTN 9 trang 119 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 118 Chân trời sáng tạo SGK
Giải KHTN 9 trang 118 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 117 Chân trời sáng tạo SGK
Giải KHTN 9 trang 117 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 116 Chân trời sáng tạo SGK
Giải KHTN 9 trang 116 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 115 Chân trời sáng tạo SGK
Giải KHTN 9 trang 115 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 114 Chân trời sáng tạo SGK
Giải KHTN 9 trang 114 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 113 Chân trời sáng tạo SGK
Giải KHTN 9 trang 113 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 112 Chân trời sáng tạo SGK
Giải KHTN 9 trang 112 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 111 Chân trời sáng tạo SGK
Giải KHTN 9 trang 111 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 110 Chân trời sáng tạo SGK
Giải KHTN 9 trang 110 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 109 Chân trời sáng tạo SGK
Giải KHTN 9 trang 109 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 108 Chân trời sáng tạo SGK
Giải KHTN 9 trang 108 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 107 Chân trời sáng tạo SGK
Giải KHTN 9 trang 107 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 106 Chân trời sáng tạo SGK
Giải KHTN 9 trang 106 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 105 Chân trời sáng tạo SGK
Giải KHTN 9 trang 105 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 104 Chân trời sáng tạo SGK
Giải KHTN 9 trang 104 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 103 Chân trời sáng tạo SGK
Giải KHTN 9 trang 103 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 102 Chân trời sáng tạo SGK
Giải KHTN 9 trang 102 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 100 Chân trời sáng tạo SGK
Giải KHTN 9 trang 100 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 99 Chân trời sáng tạo SGK
Giải KHTN 9 trang 99 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 98 Chân trời sáng tạo SGK
Giải KHTN 9 trang 98 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 97 Chân trời sáng tạo SGK
Giải KHTN 9 trang 97 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 96 Chân trời sáng tạo SGK
Giải KHTN 9 trang 96 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 95 Chân trời sáng tạo SGK
Giải KHTN 9 trang 95 Chân trời sáng tạo SGK


















































