Bài tập luyện tập tính chất hóa học của Oxit và Axit - Hóa 9 bài 5
Ở các bài học trước các em đã được tìm hiểu về tính chất hóa học của Oxit và Axit, cách điều chế và ứng dụng của một số oxit và axit quan trọng.
Bài viết này chúng ta cùng củng cố lại kiến thức về Oxit, Axit. Oxit bazo, Oxit axit và axit có tính chất hóa học nào? giữa chúng có mối quan hệ về tính chất hóa học ra sao?
I. Kiến thức cần nhớ Oxit Axit
1. Tính chất hóa học của oxit
- Tính chất hóa học của oxit được tóm tắt bằng sơ đồ dưới đây:
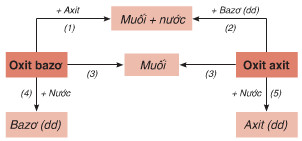
* Phản ứng hóa học minh họa:
CaO(r) + 2HCl(k) → CaCl2(dd) + H2O(l)
CO2(k) + Ca(OH)2(dd) → CaCO3(r) + H2O(l)
CaO(r) + CO2(k) → CaCO3(r)
CaO(r) + H2O(l) → Ca(OH)2(dd)
SO2(k) + H2O(l) → H2SO3(dd)
2. Tính chất hóa học của axit
- Tính chất hóa học của axit được tóm tắt bằng sơ đồ dưới đây:
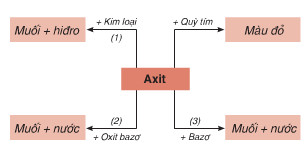
* Phản ứng hóa học minh họa:
H2SO4(dd loãng) + Fe(r) → FeSO4(dd) + H2(k)
H2SO4(dd ) + CuO(r) → CuSO4(dd) + H2O(l)
H2SO4(dd ) + 2NaOH(dd) → Na2SO4(dd) + 2H2O(l)
* Lưu ý: H2SO4 đặc có những tính chất hóa học riêng như:
- H2SO4 đặc tác dụng với nhiều kim loại không giải phóng khí hidro:
H2SO4(đặc) + Cu(r) ![\small \xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1630714419dgqprz5v10_1630796158.gif) CuSO4(dd) + 2H2O(l) + SO2(k)
CuSO4(dd) + 2H2O(l) + SO2(k)
- H2SO4 đặc có tính háo nước, hút ẩm:
C12H22O11 -H2SO4(đặc)→ 12C + 11H2O
II. Bài tập luyện tập về Oxit, Axit
* Bài 1 trang 21 SGK Hóa 9: Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với:
a) Nước. b) Axit clohidric c) Natri hiđroxit?
Viết các phương trình hóa học.
* Lời giải:
a) Những oxit tác dụng với nước: SO2, Na2O, CO2.
SO2 + H2O → H2SO3
Na2O + H2O → 2NaOH
CO2 + H2O → H2CO3
b) Những oxit tác dụng với dung dịch HCl: CuO, Na2O.
CuO + 2HCl → CuCl2 + H2O
Na2O + 2HCl → 2NaCl + H2O
c) Những oxit tác dụng với dung dịch NaOH: CO2, SO2
SO2 + 2NaOH → Na2SO3 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
* Bài 2 trang 21 SGK Hóa 9: Những oxit nào dưới đây có thể điều chế bằng:
a) Phản ứng hóa hợp? Viết phương trình hóa học.
1. H2O. 2. CuO. 3. Na2O. 4. CO2. 5. P2O5.
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
* Lời giải:
a) Cả 5 oxit đã cho có thể điều chế bằng phản ứng hóa hợp. Viết các phương trình hóa học
2H2 + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2H2O
2H2O
2Cu + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2CuO
2CuO
4Na + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2Na2O
2Na2O
4P + 5O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2P2O5
2P2O5
C + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) CO2
CO2
b) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2.
Cu(OH)2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) CuO + H2O
CuO + H2O
2Cu + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2CuO
2CuO
CaCO3 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) CaO + CO2
CaO + CO2
2Ca + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2CaO
2CaO
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
2NaNO2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) Na2O + N2 + ½ O2
Na2O + N2 + ½ O2
4Na + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2Na2O
2Na2O
Ca(HCO3)2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) CaCO3 + CO2 + H2O
CaCO3 + CO2 + H2O
2H2 + O2 ![\xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226635mcw5orta23_1630714419_1630796158.gif) 2H2O
2H2O
* Bài 3 trang 21 SGK Hóa 9: Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí CO2 và SO2. Làm thế nào có thể loại bỏ những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất? Viết các phương trình hóa học xảy ra.
* Lời giải:
- Cho hỗn hợp khí CO, CO2, SO2 lội từ từ qua dung dịch Ca(OH)2. Khi đó, CO2 và SO2 tác dụng với dung dịch Ca(OH)2 (dư) tạo kết tủa CaCO3 và CaSO3 còn lại khí CO không tác dụng thoát ra.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
SO2 + Ca(OH)2 → CaSO3↓ + H2O.
* Bài 4 trang 21 SGK Hóa 9: Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric:
a) Axit sunfuric tác dựng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích cho câu trả lời.
* Lời giải:
a) H2SO4 + CuO → CuSO4 + H2O (1)
b) Cu + 2H2SO4(đặc) → CuSO4 + SO2 ↑ + 2H2O (2)
Giả sử cần điều chế a mol CuSO4
Theo pt(1) nH2SO4 = nCuSO4 = a mol
Theo pt (2) nH2SO4 = 2.nCuSO4 = 2a mol
Do đó để tiết kiệm ta nên theo phản ứng (1) thì lượng axit H2SO4 sử dụng ít hơn ở phản ứng (2) tức là tiết kiệm axit hơn.
* Bài 5 trang 21 SGK Hóa 9: Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình phản ứng hóa học (ghi điều kiện của phản ứng, nếu có).
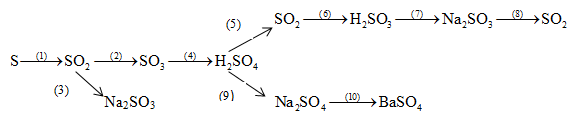 * Lời giải:
* Lời giải:
- Các phương trình phản ứng:
1) S + O2 ![xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226639es93mnnult_1630714421_1630796160.gif) SO2
SO2
2) 2SO2 + O2 ![small xrightarrow[]{t^0,V_2O_5}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1630796160iac6v7pqo4.gif) 2SO3
2SO3
3) SO2 + Na2 O → Na2SO3
4) SO3 + H2O → H2SO4
5) 2H2SO4 (đ) + Cu ![xrightarrow[]{t^0}](https://hayhochoi.vn/uploads/news/wyswyg/2021_09/1623226639es93mnnult_1630714421_1630796160.gif) CuSO4 + SO2↑ + 2H2O
CuSO4 + SO2↑ + 2H2O
6) SO2 + H2O → H2SO3
7) H2SO3 + 2NaOH → Na2SO3 + 2H2O
8) Na2SO3 + 2HCl → 2 NaCl + SO2↑ + H2O
9) H2SO4 + 2NaOH → Na2SO4 + 2H2O
10) Na2SO4 + BaCl2 → BaSO4 ↓ + 2 NaCl
Tóm lại, với nội dung bài tập luyện tập về oxit, axit hy vọng các em sẽ củng cố được kiến thức để vận dụng giải các bài tập tương tự một cách dễ dàng. Mọi câu hỏi và góp ý về bài viết các em hãy để lại dưới phần bình luận để được ghi nhận và giải đáp, chúc các em học tốt.
|
¤ Nội dung cùng chương 1: » Bài 3: Tính Chất Hóa Học Của Axit » Bài 4: Một Số Axit Quan Trọng » Bài 7: Tính Chất Hóa Học Của Bazơ » Bài 8: Một Số Bazơ Quan Trọng ¤ Có thể bạn muốn xem: |
Đánh giá & nhận xét
-
 Tính chất hoá học của Oxide, Acid, Base và Muối - Hoá lớp 9
Tính chất hoá học của Oxide, Acid, Base và Muối - Hoá lớp 9
-
 Giải KHTN 9 trang 134 Chân trời sáng tạo SGK
Giải KHTN 9 trang 134 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 132 Chân trời sáng tạo SGK
Giải KHTN 9 trang 132 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 131 Chân trời sáng tạo SGK
Giải KHTN 9 trang 131 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 130 Chân trời sáng tạo SGK
Giải KHTN 9 trang 130 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 129 Chân trời sáng tạo SGK
Giải KHTN 9 trang 129 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 128 Chân trời sáng tạo SGK
Giải KHTN 9 trang 128 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 127 Chân trời sáng tạo SGK
Giải KHTN 9 trang 127 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 126 Chân trời sáng tạo SGK
Giải KHTN 9 trang 126 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 125 Chân trời sáng tạo SGK
Giải KHTN 9 trang 125 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 124 Chân trời sáng tạo SGK
Giải KHTN 9 trang 124 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 123 Chân trời sáng tạo SGK
Giải KHTN 9 trang 123 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 122 Chân trời sáng tạo SGK
Giải KHTN 9 trang 122 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 121 Chân trời sáng tạo SGK
Giải KHTN 9 trang 121 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 120 Chân trời sáng tạo SGK
Giải KHTN 9 trang 120 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 119 Chân trời sáng tạo SGK
Giải KHTN 9 trang 119 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 118 Chân trời sáng tạo SGK
Giải KHTN 9 trang 118 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 117 Chân trời sáng tạo SGK
Giải KHTN 9 trang 117 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 116 Chân trời sáng tạo SGK
Giải KHTN 9 trang 116 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 115 Chân trời sáng tạo SGK
Giải KHTN 9 trang 115 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 114 Chân trời sáng tạo SGK
Giải KHTN 9 trang 114 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 113 Chân trời sáng tạo SGK
Giải KHTN 9 trang 113 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 112 Chân trời sáng tạo SGK
Giải KHTN 9 trang 112 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 111 Chân trời sáng tạo SGK
Giải KHTN 9 trang 111 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 110 Chân trời sáng tạo SGK
Giải KHTN 9 trang 110 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 109 Chân trời sáng tạo SGK
Giải KHTN 9 trang 109 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 108 Chân trời sáng tạo SGK
Giải KHTN 9 trang 108 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 107 Chân trời sáng tạo SGK
Giải KHTN 9 trang 107 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 106 Chân trời sáng tạo SGK
Giải KHTN 9 trang 106 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 105 Chân trời sáng tạo SGK
Giải KHTN 9 trang 105 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 104 Chân trời sáng tạo SGK
Giải KHTN 9 trang 104 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 103 Chân trời sáng tạo SGK
Giải KHTN 9 trang 103 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 102 Chân trời sáng tạo SGK
Giải KHTN 9 trang 102 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 100 Chân trời sáng tạo SGK
Giải KHTN 9 trang 100 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 99 Chân trời sáng tạo SGK
Giải KHTN 9 trang 99 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 98 Chân trời sáng tạo SGK
Giải KHTN 9 trang 98 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 97 Chân trời sáng tạo SGK
Giải KHTN 9 trang 97 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 96 Chân trời sáng tạo SGK
Giải KHTN 9 trang 96 Chân trời sáng tạo SGK
-
 Giải KHTN 9 trang 95 Chân trời sáng tạo SGK
Giải KHTN 9 trang 95 Chân trời sáng tạo SGK


















































