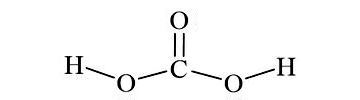
Công thức Electron của H2CO3, Công thức Lewis và CTCT của H2CO3
02:56:34Cập nhật: 22/12/2023
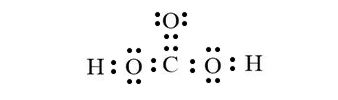
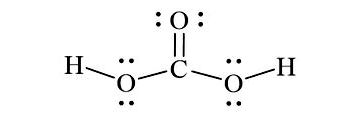
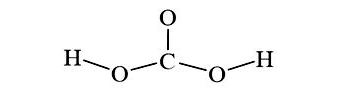
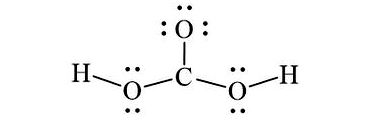
Hướng dẫn cách viết công thức Electron của H2CO3 , CTCT và công thức Lewis của H2CO3 (Carbonic Acid) và các nguyên tố hóa học theo chương trình SGK mới cực dễ hiểu.
Hy vọng với bài viết về cách viết công thức Electron của H2CO3 , công thức Lewis và CTCT của H2CO3 (Carbonic Acid) ở trên giúp các em hiểu rõ hơn về cấu trúc Lewis. Mọi góp ý và thắc mắc các em hãy để lại nhận xét dưới bài viết để HayHocHoi.Vn ghi nhận và hỗ trợ, chúc các em học tốt.
Đánh giá & nhận xét
Tin liên quan
 Orbital nguyên tử là gì? Nguyên lý Pauli và quy tắc Hund là gì? Lớp, phân lớp và cấu hình electron - Hoá 10 bài 4 CTST
Orbital nguyên tử là gì? Nguyên lý Pauli và quy tắc Hund là gì? Lớp, phân lớp và cấu hình electron - Hoá 10 bài 4 CTST Nội dung Nguyên lý PAULI là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
Nội dung Nguyên lý PAULI là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh Nội dung Quy tắc Hund là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
Nội dung Quy tắc Hund là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh Tính chất vật lí của Hydrogen Halide, tính axit của Hydrohalic, tính khử của các ion Halide - Hoá 10 bài 18 CTST
Tính chất vật lí của Hydrogen Halide, tính axit của Hydrohalic, tính khử của các ion Halide - Hoá 10 bài 18 CTST Tính chất hoá học tính chất vật lí của Halogen, đặc điểm cấu tạo, trạng thái tự nhiên và ứng dụng của Halogen - Hoá 10 bài 17 CTST
Tính chất hoá học tính chất vật lí của Halogen, đặc điểm cấu tạo, trạng thái tự nhiên và ứng dụng của Halogen - Hoá 10 bài 17 CTST Các yếu tố ảnh hưởng tới tốc độ phản ứng: Nhiệt độ, nồng độ, áp suất, bề mặt tiếp xúc, chất xúc tác và ví dụ - Hoá 10 bài 16 CTST
Các yếu tố ảnh hưởng tới tốc độ phản ứng: Nhiệt độ, nồng độ, áp suất, bề mặt tiếp xúc, chất xúc tác và ví dụ - Hoá 10 bài 16 CTST Tốc độ phản ứng hoá học là gì? Công thức biểu thức tính tốc độ phản ứng - Hoá 10 bài 15 CTST
Tốc độ phản ứng hoá học là gì? Công thức biểu thức tính tốc độ phản ứng - Hoá 10 bài 15 CTST Tính biến thiên Enthalpy của phản ứng dựa vào enthalpy tạo thành và năng lượng liên kết - Hóa 10 bài 14 CTST
Tính biến thiên Enthalpy của phản ứng dựa vào enthalpy tạo thành và năng lượng liên kết - Hóa 10 bài 14 CTST Phản ứng tỏa nhiệt là gì? Phản ứng thu nhiệt là gì? Tính biến thiên Enthalpy của phản ứng hóa học- Hóa 10 bài 13 CTST
Phản ứng tỏa nhiệt là gì? Phản ứng thu nhiệt là gì? Tính biến thiên Enthalpy của phản ứng hóa học- Hóa 10 bài 13 CTST Phản ứng Oxi hóa Khử là gì? Cách lập phương trình phản ứng Oxi hóa Khử và Ý nghĩa trong cuộc sống - Hóa 10 bài 12 CTST
Phản ứng Oxi hóa Khử là gì? Cách lập phương trình phản ứng Oxi hóa Khử và Ý nghĩa trong cuộc sống - Hóa 10 bài 12 CTST Liên kết Hydrogen là gì? Tương tác Van Der Waals là gì? Vai trò và ảnh hưởng của liên kết Hydrogen, tương tác Van der waals - Hoá 10 bài 11 CTST
Liên kết Hydrogen là gì? Tương tác Van Der Waals là gì? Vai trò và ảnh hưởng của liên kết Hydrogen, tương tác Van der waals - Hoá 10 bài 11 CTST Sự hình thành liên kết cộng hoá trị, cách viết công thức Lewis, Liên kết cho nhận và sự hình thành liên kết xích ma, liên kết pi - Hoá 10 bài 10 CTST
Sự hình thành liên kết cộng hoá trị, cách viết công thức Lewis, Liên kết cho nhận và sự hình thành liên kết xích ma, liên kết pi - Hoá 10 bài 10 CTST Liên kết ion là gì? Sự hình thành liên kết ion? Ion âm, Ion dương là gì? Tinh thể ion là gì? - Hóa 10 bài 9 CTST
Liên kết ion là gì? Sự hình thành liên kết ion? Ion âm, Ion dương là gì? Tinh thể ion là gì? - Hóa 10 bài 9 CTST Quy tắc OCTET (Bát tử) là gì? Liên kết hóa học là gì, hình thành khi nào? Vận dụng quy tắc OCTET - Hóa 10 bài 8 CTST
Quy tắc OCTET (Bát tử) là gì? Liên kết hóa học là gì, hình thành khi nào? Vận dụng quy tắc OCTET - Hóa 10 bài 8 CTST Định luật tuần hoàn, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học - Hoá 10 bài 7 CTST
Định luật tuần hoàn, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học - Hoá 10 bài 7 CTST Xu hướng biến đổi bán kính nguyên tử, độ âm điện, tính kim loại, tính phi kim, tính acid base trong chu kỳ và nhóm - Hoá 10 bài 6 CTST
Xu hướng biến đổi bán kính nguyên tử, độ âm điện, tính kim loại, tính phi kim, tính acid base trong chu kỳ và nhóm - Hoá 10 bài 6 CTST Bảng tuần hoàn các nguyên tố hoá học, phân loại nguyên tố theo cấu hình electron và tính chất hoá học - Hoá 10 bài 5 CTST
Bảng tuần hoàn các nguyên tố hoá học, phân loại nguyên tố theo cấu hình electron và tính chất hoá học - Hoá 10 bài 5 CTST Hạt nhân nguyên tử, nguyên tố hoá học là gì? Nguyên tử khối là gì? Công thức tính nguyên tử khối trung bình - Hoá 10 bài 3 CTST
Hạt nhân nguyên tử, nguyên tố hoá học là gì? Nguyên tử khối là gì? Công thức tính nguyên tử khối trung bình - Hoá 10 bài 3 CTST Cấu tạo nguyên tử, hạt nhân nguyên tử, thí nghiệm của Thomson và Rutherford - Hoá 10 bài 2 CTST
Cấu tạo nguyên tử, hạt nhân nguyên tử, thí nghiệm của Thomson và Rutherford - Hoá 10 bài 2 CTST Đối tượng nghiên cứu của hoá học, vai trò của hoá học trong đời sống sản xuất và phương pháp học - Hoá 10 bài 1 CTST
Đối tượng nghiên cứu của hoá học, vai trò của hoá học trong đời sống sản xuất và phương pháp học - Hoá 10 bài 1 CTST Mục lục Sách giáo khoa (SGK) Hoá 10 Chân trời sáng tạo - Lý thuyết và bài tập Hóa học 10 CTST
Mục lục Sách giáo khoa (SGK) Hoá 10 Chân trời sáng tạo - Lý thuyết và bài tập Hóa học 10 CTST Công thức Electron của HClO2, Công thức Lewis và CTCT của HClO2
Công thức Electron của HClO2, Công thức Lewis và CTCT của HClO2 Công thức Electron của HClO, Công thức Lewis và CTCT của HClO
Công thức Electron của HClO, Công thức Lewis và CTCT của HClO Công thức Electron của C2H2, Công thức Lewis và CTCT của C2H2
Công thức Electron của C2H2, Công thức Lewis và CTCT của C2H2 Công thức Electron của CO2, Công thức Lewis và CTCT của CO2
Công thức Electron của CO2, Công thức Lewis và CTCT của CO2 Công thức Electron của BH3, Công thức Lewis và CTCT của BH3
Công thức Electron của BH3, Công thức Lewis và CTCT của BH3 Công thức Electron của SF4, Công thức Lewis và CTCT của SF4
Công thức Electron của SF4, Công thức Lewis và CTCT của SF4 Viết công thức Electron, công thức Lewis và CTCT của nước H2O
Viết công thức Electron, công thức Lewis và CTCT của nước H2O Viết công thức Electron, công thức Lewis và CTCT của Nitrogen N2
Viết công thức Electron, công thức Lewis và CTCT của Nitrogen N2 Viết công thức Electron, công thức Lewis và CTCT của SF6 (Sulfur hexafluoride)
Viết công thức Electron, công thức Lewis và CTCT của SF6 (Sulfur hexafluoride)
Tin mới
Tin cùng chuyên mục
Tin xem nhiều nhất