Định luật tuần hoàn Men-đê-lê-ép, Độ âm điện, Sự biến đổi tính chất trong 1 Chu kỳ, 1 Nhóm - Hóa 10 bài 9
Theo chiều tăng điện tích hạt nhân của nguyên tử các nguyên tố, tính kim loại và phi kim của các nguyên tố biến đổi ra sao? Hóa trị của các nguyên tố có thay đổi theo quy luật nào không? Thành phần và tính chất của hợp chất các nguyên tố biến đổi như thế nào?
Để trả lời câu hỏi trên, bài viết này chúng ta cùng tìm hiểu về Định luật tuần hoàn Men-đê-lê-ép (Mendeleev) được phát biểu ra sao? Sự biến đổi trong 1 chu kỳ, trong một nhóm A của các nguyên tố trong bảng tuần hoàn theo quy luật nào? Độ âm điện của Flo, Oxi, Na,... là bao nhiêu và Độ âm điện của một nguyên tử đặc trưng cho khả năng gì?
I. Tính kim loại, tính phi kim
- Tính kim loại là tính chất của một nguyên tố mà nguyên tử của nó dễ mất electron để trở thành ion dương.
- Kim loại càng mạnh khi khả năng mất electron càng lớn.
- Tính phi kim là tính chất của một nguyên tố mà nguyên tử của nó dễ thu electron để trở thành ion âm.
- Phi kim càng mạnh khi khả năng nhận electron càng lớn.
1. Sự biến đổi tính chất trong 1 chu kỳ
- Trong một chu kì, theo chiều tăng dần của điện tính hạt nhân, tính kim loại giảm dần, tính phi kim tăng dần.
- Trong 1 chu kỳ, khi đi từ trái sang phải, điện tích hạt nhân tăng dần, số lớp electron không đổi, lực hút giữa hạt nhân và electron lớp ngoài cùng tăng, làm cho bán kính nguyên tử giảm, khả năng mất electron giảm, khả năng nhận electron tăng.
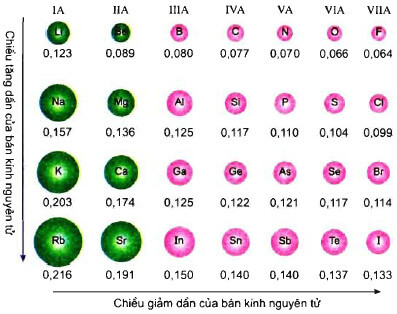
2. Sự biến đổi tính chất trong một nhóm A
- Trong một nhóm A theo chiều tăng dần điện tích hạt nhân, tính kim loại tăng dần, tính phi kim giảm dần.
- Trong một nhóm A, theo chiều từ trên xuống dưới, điện tích hạt nhân tăng, số lớp electron cũng tăng dần, làm cho bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, khả năng mất electron tăng (tính kim loại tăng), khả năng nhận electron giảm (tính phi kim giảm).
3. Độ âm điện là gì?
a) Khái niệm độ âm điện
- Độ âm điện của một nguyên tử đặc trưng cho khả năng hút electron của nguyên tử đó khi hình thành liên kết hóa học.
b) Bảng độ âm điện của nguyên tử một số nguyên tố
- Trong một chu kì theo chiều tăng dần của điện tích hạt nhân giá trị độ âm điện tăng dần
- Trong một nhóm A theo chiều tăng dần của diện tích hạt nhân, giá trị độ âm điện giảm dần.
- Quy luật biến đổi độ âm điện phù hợp với sự biến đổi tính kim loại, tính phi kim của các nguyên tố trong 1 chu kỳ và trong một nhóm A.
- Kết luận: Tính kim loại, tính phi kim của các nguyên tố biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân.
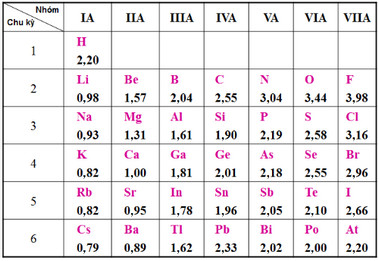 Bảng độ âm điện của nguyên tử một số nguyên tố
Bảng độ âm điện của nguyên tử một số nguyên tố
- Độ âm điện của một nguyên tố càng lớn thì tính phi kim càng mạnh, tính kim loại càng giảm và ngược lại.
* Ví dụ: Từ bảng độ âm điện của nguyên tử một số nguyên tố ở trên ta thấy:
- Độ âm điện của Na là: 0,93
- Độ âm điện của Flo là: 3,98
- Độ âm điện của Oxi là: 3,44
3. Hóa trị của các nguyên tố
- Trong chu kì 3 đi từ trái sang phải, hóa trị cao nhất của các nguyên tố đối với oxi tăng từ 1 đến 7 còn hóa trị trong hợp chất khí đối với hiđro giảm từ 4 đến 1
- Trong chu kì hóa trị cao nhất của các nguyên tố đối với oxi tăng dần và hiđro giảm dần
* Bảng minh họa sự biến đổi tuần hóa trị của các nguyên tố
| STT nhóm A | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| Hợp chất với Oxi | Na2O, K2O | MgO, CaO | Al2O3, Ga2O3 | SiO2, GeO2 | P2O5, As2O5 | SO3, SeO3 | Cl2O7, Br2O7 |
| Hóa trị cao nhất với Oxi | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Hợp chất khí với Hidro | SiH4, GeH4 | PH3, AsH | 3H2S, H2Se | HCl, HBr | |||
| Hóa trị với hidro | 4 | 3 | 2 | 1 |
III. Oxit và Hidroxit của các nguyên tố nhóm A thuộc cùng chu kỳ
- Trong một chu kỳ, đi từ trái sang phải theo chiều tăng của điện tích hạt nhân, tính bazơ của các oxit và hiđroxit giảm dần đồng thời tính axit của chúng tăng dần.
|
Na2O Oxit bazơ |
MgO Oxit bazơ |
Al2O3 Oxit lưỡng tính |
SiO2 Oxit axit |
P2O5 Oxit axit |
SO3 Oxit axit |
Cl2O7 Oxit axit |
|
NaOH Bazơ mạnh (kiềm) |
Mg(OH)2 Bazơ yếu |
Al(OH)3 Bazơ lưỡng tính |
H2SiO3 Axit yếu |
H3PO4 Axit trung bình |
H2SO4 Axit mạnh |
HClO4 Axit rất mạnh |
IV. Định luật tuần hoàn Men-đê-lê-ép (Mendeleev)
- Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng dần của điện tích hạt nhân nguyên tử.
V. Bài tập về định luận tuần hoàn và sự biến đổi tính chất của các nguyên tố
* Bài 1 trang 47 SGK Hóa 10: Trong một chu kì, bán kính nguyên tử các nguyên tố.
A. Tăng theo chiều tăng dần của điện tích hạt nhân.
B. Giảm theo chiều tăng dần của điện tích hạt nhân.
C. Giảm theo chiều tăng của tính phi kim.
D. B và C đều đúng.
Chọn đáp án đúng nhất.
° Lời giải bài 1 trang 47 SGK Hóa 10:
• Chọn đáp án: D. B và C đều đúng.
* Bài 2 trang 47 SGK Hóa 10: Trong một nhóm A, bán kính nguyên tử của các nguyên tố:
A. Tăng theo chiều tăng dần của điện tích hạt nhân.
B. Giảm theo chiều tăng dần của điện tích hạt nhân.
C. Giảm theo chiều tăng của tính kim loại.
D. B và C đều đúng.
Chọn đáp án đúng nhất.
° Lời giải bài 2 trang 47 SGK Hóa 10:
• Chọn đáp án: A. Tăng theo chiều tăng dần của điện tích hạt nhân.
* Bài 3 trang 47 SGK Hóa 10: Những tính chất nào sau đây biến đổi tuần hoàn?
a) Hóa trị cao nhất với oxi.
b) Nguyên tử khối.
c) Số electron lớp ngoài cùng.
d) Số lớp electron.
e) Số electron trong nguyên tử.
° Lời giải bài 3 trang 47 SGK Hóa 10:
• Những tính chất sau đây biến đổi tuần hoàn.
a) Hóa trị cao nhất với oxi.
c) Số electron lớp ngoài cùng.
* Bài 4 trang 47 SGK Hóa 10: Các nguyên tố halogen được sắp xếp theo chiều bán kính nguyên tử giảm dần (từ trái sang phải) như sau
A. I, Br, Cl, F. B. F, Cl, Br, I.
C. I, Br, F, Cl. D. Br, I, Cl, F.
Chọn đáp án đúng
° Lời giải bài 4 trang 47 SGK Hóa 10:
• Chọn đán án đúng: A. I, Br, Cl, F;
* Bài 5 trang 48 SGK Hóa 10: Các nguyên tố của chu kì 2 được sắp xếp theo chiều giá trị độ âm điện giảm dần theo thứ tự từ trái sang phải như sau:
A. F, O, N, C, B, Be, Li.
B. Li, B, Be, N, C, F, O.
C. Be, Li, C, B, O, N, F.
D. N, O, F, Li, Be, B, C.
Chọn đáp án đúng.
° Lời giải bài 5 trang 48 SGK Hóa 10:
• Chọn đán án đúng: A. F, O, N, C, B, Be, Li.
* Bài 6 trang 48 SGK Hóa 10: Oxit cao nhất của 1 nguyên tố R ứng với công thức RO2. Nguyên tố R đó là
A. Magie B. Nitơ C. Cacbon D. Photpho.
Chọn đáp án đúng.
° Lời giải bài 6 trang 48 SGK Hóa 10:
• Chọn đán án đúng: C. Cacbon
- Vì Nitơ và photpho có oxit cao nhất dạng R2O5 trong khi Magie là RO.
* Bài 7 trang 48 SGK Hóa 10: Theo quy luật biến đổi tính chất đơn chất của các nguyên tố trong bảng tuần hoàn thì:
A. Phi kim mạnh nhất là iot.
B. Kim loại mạnh nhất là liti.
C. Phi kim mạnh nhất là flo.
D. Kim loại yêu nhất là xesi.
Chọn đáp án đúng
° Lời giải bài 7 trang 48 SGK Hóa 10:
• Chọn đán án đúng: C. Phi kim mạnh nhất là flo.
* Bài 8 trang 48 SGK Hóa 10: Viết cấu hình electron của nguyên tử magie (Z = 12). Để đạt được cấu hình electron nguyên tử của khí hiếm gần nhất trong bảng tuần hoàn, nguyên tử magie nhân hay nhường bao nhiêu electron? Magie thể hiện tính chất kim loại hay phi kim?
° Lời giải bài 8 trang 48 SGK Hóa 10:
- Cấu hình electron của nguyên tử Mg (Z = 12) là: 1s22s22p63s2.
- Để đạt cấu hình electron của khí hiếm gần nhất (Ne) trong Bảng tuần hoàn nguyên tử Mg nhường 2 electron để đạt 8e ở lớp ngoài cùng.
- Mg có tính kim loại: Mg – 2e → Mg2+
* Bài 9 trang 48 SGK Hóa 10: Viết cấu hình electron nguyên tử của lưu huỳnh S (Z = 16). Để đạt được cấu hình electron của khí hiếm gần nhất trong bảng tuần hoàn, nguyên tử lưu huỳnh nhận hay nhường bao nhiêu electron? Lưu huỳnh thể hiện tính chất kim loại hay phi kim?
° Lời giải bài 9 trang 48 SGK Hóa 10:
- Cấu hình electron của nguyên tử S (Z = 16) là: 1s22s22p63s23p4.
- Để đạt cấu hình electron của khí hiếm gần nhất (Ar) trong Bảng tuần hoàn nguyên tử S nhận 2 electron để đạt 8e ở lớp ngoài cùng.
- S có tính phi kim: S + 2e → S2-
* Bài 10 trang 48 SGK Hóa 10: Độ âm điện của một nguyên tử là gì? Gía trị độ âm điện của nguyên tử các nguyên tố trong các nhóm A biến đổi như thế nào theo chiều điện tích hạt nhân tăng?
° Lời giải bài 10 trang 48 SGK Hóa 10:
- Độ âm điện của một nguyên tố đặc trưng cho khả năng hút electron của nguyên tử nguyên tố đó trong phân tử (những electron bị hút là những electron nằm trong liên kết giữa các nguyên tử trong phân tử).
- Độ âm điện của nguyên tử các nguyên tố trong các nhóm A giảm dần theo chiều tăng của điện tích hạt nhân.
* Ví dụ: Độ âm điện giảm theo chiều tăng điện tích hạt nhân
| Nhóm IA | 3Li | 11Na | 19K | 37Pb | 35Co |
| Độ âm điện | 1 | 0,9 | 0,8 | 0,8 | 0,7 |
* Bài 11 trang 48 SGK Hóa 10: Nguyên tử của nguyên tố nào có giá trị độ âm điện lớn nhất? Tại sao?
° Lời giải bài 11 trang 48 SGK Hóa 10:
• Nguyên tử của nguyên tố Flo có giá trị độ âm điện lớn nhất vì:
- Flo là phi kim mạnh nhất.
- Trong cùng một chu kỳ, các nguyên tử của các nguyên tố nhóm VIIA có độ âm điện lớn nhất (độ âm điện tăng từ trái qua phải).
- Trong cùng một nhóm A, độ âm điện của nguyên tử nguyên tố đứng đầu là lớn nhất (độ âm điện giảm từ trên xuống dưới).
* Bài 12 trang 48 SGK Hóa 10: Cho hai dãy chất sau:
Li2O; BeO; B2O3; CO2; N2O5.
CH4; NH3; H2O; HF.
Xác định hóa trị của các nguyên tố với oxi và với hiđro.
° Lời giải bài 12 trang 48 SGK Hóa 10:
• Trong dãy chất:
Li2O; BeO; B2O3; CO2; N2O5.
- Hóa trị cao nhất với oxi tăng dần từ I đến V.
• Trong dãy chất:
CH4; NH3; H2O; HF.
- Hóa trị với hidro giảm dần từ IV xuống I.
Hy vọng với bài viết về Định luật tuần hoàn Men-đê-lê-ép, Độ âm điện, Sự biến đổi tính chất trong 1 Chu kỳ, 1 Nhóm ở trên hữu ích cho các em. Mọi góp ý và thắc mắc các em vui lòng để lại nội dung dưới phần bình luận để HayHocHoi.Vn ghi nhận và hỗ trợ, chúc các em học tập tốt.
¤ Xem thêm các bài viết khác tại:
Đánh giá & nhận xét
-
 Nội dung Quy tắc Hund là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
Nội dung Quy tắc Hund là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
-
 Nội dung Nguyên lý PAULI là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
Nội dung Nguyên lý PAULI là gì, Ví dụ, Hóa 10 - Hỏi đáp nhanh
-
 Ôn tập chương 7: Nguyên tố nhóm Halogen? Hóa 10 bài 23 KNTT (Kết nối tri thức)
Ôn tập chương 7: Nguyên tố nhóm Halogen? Hóa 10 bài 23 KNTT (Kết nối tri thức)
-
 Tính chất hóa học của HydroHalic acid, muối Halide? Cấu tạo và tính chất vật lí của hydrogen Halide? Hóa 10 bài 22 KNTT
Tính chất hóa học của HydroHalic acid, muối Halide? Cấu tạo và tính chất vật lí của hydrogen Halide? Hóa 10 bài 22 KNTT
-
 Tính chất hóa học, tính chất vật lí của Halogen? Trạng thái tự nhiên, Cấu tạo nguyên tử Halogen? Hóa 10 bài 21 KNTT
Tính chất hóa học, tính chất vật lí của Halogen? Trạng thái tự nhiên, Cấu tạo nguyên tử Halogen? Hóa 10 bài 21 KNTT
-
 Ôn tập chương 6: Tốc độ phản ứng? Hóa 10 bài 20 KNTT (Kết nối tri thức)
Ôn tập chương 6: Tốc độ phản ứng? Hóa 10 bài 20 KNTT (Kết nối tri thức)
-
 Tốc độ phản ứng là gì? Các yếu tố ảnh hưởng tới tốc độ của phản ứng? Hóa 10 bài 19 KNTT
Tốc độ phản ứng là gì? Các yếu tố ảnh hưởng tới tốc độ của phản ứng? Hóa 10 bài 19 KNTT
-
 Ôn tập chương 5: Biến thiên Enthalpy trong các phản ứng hóa học? Hóa 10 bài 18 KNTT (Kết nối tri thức)
Ôn tập chương 5: Biến thiên Enthalpy trong các phản ứng hóa học? Hóa 10 bài 18 KNTT (Kết nối tri thức)
-
 Phản ứng tỏa nhiệt, phản ứng thu nhiệt là gì? Ý nghĩa Biến thiên Enthalpy là gì? Hóa 10 bài 17 KNTT
Phản ứng tỏa nhiệt, phản ứng thu nhiệt là gì? Ý nghĩa Biến thiên Enthalpy là gì? Hóa 10 bài 17 KNTT
-
 Ôn tập chương 4: Phản ứng oxi hóa - khử? Hóa 10 bài 16 KNTT (Kết nối tri thức)
Ôn tập chương 4: Phản ứng oxi hóa - khử? Hóa 10 bài 16 KNTT (Kết nối tri thức)
-
 Phản ứng Oxi hóa - khử? Quy tắc xác định số Oxi hóa, chất oxi hóa, chất khử, lập PTHH ôxi hóa khử? Hóa 10 bài 15 KNTT
Phản ứng Oxi hóa - khử? Quy tắc xác định số Oxi hóa, chất oxi hóa, chất khử, lập PTHH ôxi hóa khử? Hóa 10 bài 15 KNTT
-
 Ôn tập chương 3: Liên kết hóa học? Hóa 10 bài 14 KNTT (Kết nối tri thức)
Ôn tập chương 3: Liên kết hóa học? Hóa 10 bài 14 KNTT (Kết nối tri thức)
-
 Bản chất liên kết Hydrogen? Khái niệm tương tác Van der Waals và sự ảnh hưởng? Hóa 10 bài 13 KNTT
Bản chất liên kết Hydrogen? Khái niệm tương tác Van der Waals và sự ảnh hưởng? Hóa 10 bài 13 KNTT
-
 Sự tạo thành liên kết cộng hóa trị? Phân tử có liên kết đơn, liên kết đôi và liên kết ba? Hóa 10 bài 12 KNTT
Sự tạo thành liên kết cộng hóa trị? Phân tử có liên kết đơn, liên kết đôi và liên kết ba? Hóa 10 bài 12 KNTT
-
 Liên kết ion là gì? Sự tạo thành liên kết ion, tinh thể ion, tính chất của hợp chất ion? Hóa 10 bài 11 KNTT
Liên kết ion là gì? Sự tạo thành liên kết ion, tinh thể ion, tính chất của hợp chất ion? Hóa 10 bài 11 KNTT
-
 Quy tắc OCTET, Khái niệm liên kết hóa học? Hóa 10 bài 10 KNTT
Quy tắc OCTET, Khái niệm liên kết hóa học? Hóa 10 bài 10 KNTT
-
 Ôn tập chương 2: Bảng tuần hoàn các nguyên tố hóa học, Định luật tuần hoàn? Hóa 10 bài 9 KNTT (Kết nối tri thức)
Ôn tập chương 2: Bảng tuần hoàn các nguyên tố hóa học, Định luật tuần hoàn? Hóa 10 bài 9 KNTT (Kết nối tri thức)
-
 Định luật tuần hoàn Mendeleev, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học? Hóa 10 bài 8 KNTT
Định luật tuần hoàn Mendeleev, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học? Hóa 10 bài 8 KNTT
-
 Tính chất của các Oxide và Hydroxide, Thành phẩn của các Oxide và Hydroxide? Hóa 10 bài 7 KNTT
Tính chất của các Oxide và Hydroxide, Thành phẩn của các Oxide và Hydroxide? Hóa 10 bài 7 KNTT
-
 Độ âm điện của nguyên tử là gì? Sự biến đổi tính kim loại và tính phi kim trong một nhóm, chu kỳ? Hóa 10 bài 6 KNTT
Độ âm điện của nguyên tử là gì? Sự biến đổi tính kim loại và tính phi kim trong một nhóm, chu kỳ? Hóa 10 bài 6 KNTT
-
 Cấu tạo bảng tuần hoàn, nguyên tắc sắp xếp các nguyên tố, ô nguyên tố, chu kì, nhóm? Hóa 10 bài 5 KNTT
Cấu tạo bảng tuần hoàn, nguyên tắc sắp xếp các nguyên tố, ô nguyên tố, chu kì, nhóm? Hóa 10 bài 5 KNTT
-
 Ôn tập chương 1: Cấu tạo nguyên tử? Hóa 10 bài 4 KNTT (Kết nối tri thức)
Ôn tập chương 1: Cấu tạo nguyên tử? Hóa 10 bài 4 KNTT (Kết nối tri thức)
-
 Cách viết cấu hình Electron nguyên tử? Biểu diễn cấu hình E theo orbital? đặc điểm lớp E ngoài cùng? Hóa 10 bài 3 KNTT
Cách viết cấu hình Electron nguyên tử? Biểu diễn cấu hình E theo orbital? đặc điểm lớp E ngoài cùng? Hóa 10 bài 3 KNTT
-
 Nguyên tử khối là gì? Công thức tính nguyên tử khối trung bình? Kí hiệu nguyên tử, nguyên tố hóa học? Hóa 10 bài 2 KNTT
Nguyên tử khối là gì? Công thức tính nguyên tử khối trung bình? Kí hiệu nguyên tử, nguyên tố hóa học? Hóa 10 bài 2 KNTT
-
 Cấu tạo Nguyên tử? Kích thước, khối lượng của nguyên tử, điện tích hạt nhân và số khối? Hóa 10 bài 1 KNTT
Cấu tạo Nguyên tử? Kích thước, khối lượng của nguyên tử, điện tích hạt nhân và số khối? Hóa 10 bài 1 KNTT
-
 Đối tượng nghiên cứu hóa học, vai trò của hóa học trong đời sống sản xuất và cách học? Hóa 10 bài mở đầu KNTT
Đối tượng nghiên cứu hóa học, vai trò của hóa học trong đời sống sản xuất và cách học? Hóa 10 bài mở đầu KNTT
-
 Mục lục SGK Hóa 10 Kết nối tri thức - Lý thuyết và bài tập Hóa 10 SGK Kết nối tri thức
Mục lục SGK Hóa 10 Kết nối tri thức - Lý thuyết và bài tập Hóa 10 SGK Kết nối tri thức
-
 Tính chất vật lí của Hydrogen Halide, tính axit của Hydrohalic, tính khử của các ion Halide - Hoá 10 bài 18 CTST
Tính chất vật lí của Hydrogen Halide, tính axit của Hydrohalic, tính khử của các ion Halide - Hoá 10 bài 18 CTST
-
 Tính chất hoá học tính chất vật lí của Halogen, đặc điểm cấu tạo, trạng thái tự nhiên và ứng dụng của Halogen - Hoá 10 bài 17 CTST
Tính chất hoá học tính chất vật lí của Halogen, đặc điểm cấu tạo, trạng thái tự nhiên và ứng dụng của Halogen - Hoá 10 bài 17 CTST
-
 Các yếu tố ảnh hưởng tới tốc độ phản ứng: Nhiệt độ, nồng độ, áp suất, bề mặt tiếp xúc, chất xúc tác và ví dụ - Hoá 10 bài 16 CTST
Các yếu tố ảnh hưởng tới tốc độ phản ứng: Nhiệt độ, nồng độ, áp suất, bề mặt tiếp xúc, chất xúc tác và ví dụ - Hoá 10 bài 16 CTST
-
 Tốc độ phản ứng hoá học là gì? Công thức biểu thức tính tốc độ phản ứng - Hoá 10 bài 15 CTST
Tốc độ phản ứng hoá học là gì? Công thức biểu thức tính tốc độ phản ứng - Hoá 10 bài 15 CTST
-
 Tính biến thiên Enthalpy của phản ứng dựa vào enthalpy tạo thành và năng lượng liên kết - Hóa 10 bài 14 CTST
Tính biến thiên Enthalpy của phản ứng dựa vào enthalpy tạo thành và năng lượng liên kết - Hóa 10 bài 14 CTST
-
 Phản ứng tỏa nhiệt là gì? Phản ứng thu nhiệt là gì? Tính biến thiên Enthalpy của phản ứng hóa học- Hóa 10 bài 13 CTST
Phản ứng tỏa nhiệt là gì? Phản ứng thu nhiệt là gì? Tính biến thiên Enthalpy của phản ứng hóa học- Hóa 10 bài 13 CTST
-
 Phản ứng Oxi hóa Khử là gì? Cách lập phương trình phản ứng Oxi hóa Khử và Ý nghĩa trong cuộc sống - Hóa 10 bài 12 CTST
Phản ứng Oxi hóa Khử là gì? Cách lập phương trình phản ứng Oxi hóa Khử và Ý nghĩa trong cuộc sống - Hóa 10 bài 12 CTST
-
 Liên kết Hydrogen là gì? Tương tác Van Der Waals là gì? Vai trò và ảnh hưởng của liên kết Hydrogen, tương tác Van der waals - Hoá 10 bài 11 CTST
Liên kết Hydrogen là gì? Tương tác Van Der Waals là gì? Vai trò và ảnh hưởng của liên kết Hydrogen, tương tác Van der waals - Hoá 10 bài 11 CTST
-
 Sự hình thành liên kết cộng hoá trị, cách viết công thức Lewis, Liên kết cho nhận và sự hình thành liên kết xích ma, liên kết pi - Hoá 10 bài 10 CTST
Sự hình thành liên kết cộng hoá trị, cách viết công thức Lewis, Liên kết cho nhận và sự hình thành liên kết xích ma, liên kết pi - Hoá 10 bài 10 CTST
-
 Liên kết ion là gì? Sự hình thành liên kết ion? Ion âm, Ion dương là gì? Tinh thể ion là gì? - Hóa 10 bài 9 CTST
Liên kết ion là gì? Sự hình thành liên kết ion? Ion âm, Ion dương là gì? Tinh thể ion là gì? - Hóa 10 bài 9 CTST
-
 Quy tắc OCTET (Bát tử) là gì? Liên kết hóa học là gì, hình thành khi nào? Vận dụng quy tắc OCTET - Hóa 10 bài 8 CTST
Quy tắc OCTET (Bát tử) là gì? Liên kết hóa học là gì, hình thành khi nào? Vận dụng quy tắc OCTET - Hóa 10 bài 8 CTST
-
 Định luật tuần hoàn, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học - Hoá 10 bài 7 CTST
Định luật tuần hoàn, Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học - Hoá 10 bài 7 CTST